Черные и цветные металлы
Металлами называются химически простые вещества, отличающиеся хорошим блеском, высокими теплои электропроводностью, непрозрачностью, плавкостью. Некоторые из металлов можно ковать и сваривать.
К черным относят железо и сплавы на его основе — чугун и сталь, а также ферросплавы. Остальные металлы составляют группу цветных. Из цветных металлов наиболее важное промышленное значение имеют медь, алюминий, свинец, олово, никель, титан и др. Цветные металлы обладают рядом физико-химических свойств, которые делают их незаменимыми в технике. В настоящее время широко применяют редкие цветные металлы: галлий, индий, бериллий, церий, цезий, неодим и другие, обладающие очень высокими физико-химическими и механическими свойствами как в чистом виде, так и в составе соединений с другими металлами. Галлий, имея низкую температуру плавления (29,8°С), кипит при температуре 2230°С; он широко используется для изготовления термометров, предназначенных для измерения высоких температур.
Индий обладает высокой отражательной способностью равномерно рассеивать свет и используется для изготовления зеркал и прожекторов. Тонкий слой индия защищает ветровые стекла от обледенения.
Бериллий — самый прочный из всех легких металлов. Его плотность 1,84 г/см3, он легче алюминия в 1,5 раза, а по удельной прочности превосходит алюминий в пять раз, а титан — в три раза. Бериллий обладает высокими акустическими свойствами. Скорость звука в нем распространяется в 2,5 раза быстрее, чем в стали. Бериллий необходим для использования в атомной технике. Бериллиевая бронза используется в машиностроении и других отраслях промышленности.
Литий применяется в ядерной технике, радиотехнике. Смазочный материал на основе оксида лития не замерзает при температуре –50°С.
Ниобий обладает высокой кислотостойкостью, он чрезвычайно пластичен, его можно обрабатывать на холоде, температура плавления ниобия 2500°С. Из сплава ниобия с цезием изготовляют центральную часть атомного реактора.
Тантал — тугоплавкий металл, температура его плавления 2996°С, он коррозионно-стоек, применяется в виде пластинок и проволоки в костной и пластической хирургии.
Осмий — один из самых тяжелых и твердых металлов, очень износоустойчив, используется для изготовления хирургических инструментов, позолоченных перьев в авторучках, долгоиграющих игл, осей и опор точных измерительных приборов и часовых механизмов.
Что такое металл и чем он отличается от неметалла?
Иными словами, как можно понять, что перед нами находится металлический материал? Ответы на все эти вопросы можно получить, если рассмотреть уникальные свойства металлов. К ним относятся следующие основные:
- Наличие металлического блеска при полировке поверхности. Все металлы блестят, в своем большинстве они имеют серый цвет, однако, некоторые металлы обладают специфической окраской, например, висмут розовый, медь красноватая, а золото желтое.
- Высокая теплопроводность и электропроводность. При комнатной температуре наиболее высокие показатели для этих физических свойств характерны для меди и серебра.
- При комнатной температуре практически все металлы находятся в твердом агрегатном состоянии материи. Исключение составляет ртуть, которая плавится уже при -39 oC.
- Будучи в твердом состоянии, металлы кристаллическим строением характеризуются. Если расплав рассматриваемого материала слишком быстро охлаждать, то он приобретает аморфную структуру, в которой все же сохраняется ближний порядок.
- Температуры плавления и плотности металлов варьируются в широких пределах. Так, элемент вольфрам является самым тугоплавким (3410 oC). Самым же тяжелым считается осмий (в 22,6 раза плотнее воды), а самым легким — литий (почти в 2 раза менее плотный, чем вода).
- Все металлы химически активны. Поскольку они обладают низкой электроотрицательностью, то в химических реакциях их атомы отдают электроны и превращаются в положительно заряженные ионы (катионы).
Выше в списке были перечислены основные свойства металлов, которые их отличают от неметаллических материалов. Примерами последних являются кислород, азот, благородные газы, сера, кремний, углерод и некоторые другие. Заметим, что все живые организмы состоят в основном из неметаллов.
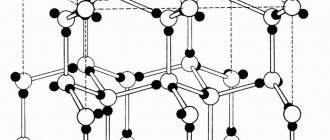
Типы кристаллических решеток
Кристаллическая решетка — это воображаемая пространственная сетка, в узлах которой располагаются атомы (ионы), образующие металл. Частицы вещества (ионы, атомы), из которых построен кристалл, расположены в определенном геометрическом порядке, который периодически повторяется в пространстве.
В аморфных телах (стекле, пластмассах), в отличие от кристаллов, атомы или молекулы расположены беспорядочно, хаотично.
Формирование кристаллической решетки в металле происходит следующим образом:
- при переходе металла из жидкого в твердое состояние расстояние между атомами сокращается, а силы взаимодействия между ними возрастают;
- при сближении атомов электроны, находящиеся на внешних оболочках, теряют связь со своими атомами вследствие отрыва валентного электрона одного атома положительно заряженным ядром другого и т.д.;
- происходит образование свободных электронов, так как они не принадлежат отдельным атомам.
Таким образом, в твердом состоянии металл представляет собой структуру, состоящую из положительно заряженных ионов, вокруг которых движутся свободные электроны. Связь в металле осуществляется электростатическими силами. Между ионами и свободными электронами возникают электростатические силы притяжения, которые «стягивают» ионы. Такую связь между частицами металла называют металлической.
Силы связи в металлах определяются силами отталкивания и силами притяжения между ионами и электронами. Ионы находятся на таком расстоянии один от другого, при котором потенциальная энергия взаимодействия минимальна. В металле ионы располагаются в определенном порядке, образуя кристаллическую решетку. Такое расположение ионов обеспечивается взаимодействием их с валентными электронами, которые связывают ионы в кристаллической решетке. Типы кристаллических решеток у различных металлов различны. Наиболее часто встречаются решетки: объемно-центрированная кубическая (ОЦК) — -Fe, Cr, W, гранецентрированная кубическая (ГЦК) — -Fe, Al, Сu и гексагональная плотно упакованная (ГПУ) — Mg, Zn и др.
Наименьший объем кристалла, дающий представление об атомной структуре металла в любом его объеме, называют элементарной кристаллической ячейкой.
Внутреннее строение и физические свойства металлов
Металлы — это простые вещества, атомы которых могут только отдавать электроны. Такая особенность металлов связана с тем, что на внешнем уровне этих атомов мало электронов (чаще всего от 1 до 3) или внешние электроны расположены далеко от ядра. Чем меньше электронов на внешнем уровне атома и чем дальше они расположены от ядра, — тем активнее металл (ярче выражены его металлические свойства).
Задание 8.1. Какой металл активнее:
Назовите химические элементы А, Б, В, Г.
Металлы и неметаллы в Периодической системе химических элементов Менделеева (ПСМ) разделяет линия, проведённая от бора к астату. Выше этой линии в главных подгруппах находятся неметаллы (см. урок 3). Остальные химические элементы — металлы.
Задание 8.2. Какие из следующих элементов относятся к металлам: кремний, свинец, сурьма, мышьяк, селен, хром, полоний?
Вопрос. Как можно объяснить тот факт, что кремний — неметалл, а свинец — металл, хотя число внешних электронов у них одинаково?
Существенной особенностью атомов металлов является их большой радиус и наличие слабо связанных с ядром валентных электронов. Для таких атомов величина энергии ионизации* невелика.
* ЭНЕРГИЯ ИОНИЗАЦИИ равна работе, затрачиваемой на удаление одного внешнего электрона из атома (на ионизацию атома), находящегося в основном энергетическом состоянии.
Часть валентных электронов металлов, отрываясь от атомов, становятся «свободными». «Свободные» электроны легко перемещаются между атомами и ионами металлов в кристалле, образуя «электронный газ» (рис. 28).
В последующий момент времени любой из «свободных» электронов может притянуться любым катионом, а любой атом металла может отдать электрон и превратиться в ион (эти процессы показаны на рис. 28 пунктирами).
Таким образом, внутреннее строение металла похоже на слоёный пирог, где положительно заряженные «слои» атомов и ионов металла чередуются с электронными «прослойками» и притягиваются к ним. Наилучшей моделью внутреннего строения металла является стопка стеклянных пластинок, смоченных водой: оторвать одну пластинку от другой очень трудно (металлы прочные), а сдвинуть одну пластинку относительно другой очень легко (металлы пластичные) (рис. 29).
Задание 8.3. Сделайте такую «модель» металла и убедитесь в этих свойствах.
Химическая связь, осуществляемая за счёт «свободных» электронов, называется металлической связью.
«Свободные» электроны обеспечивают также такие физические свойства металлов, как электро- и теплопроводность, пластичность (ковкость), а также металлический блеск.
Задание 8.4. Найдите дома металлические предметы.
Выполняя это задание, вы легко найдёте на кухне металлическую посуду: кастрюли, сковородки, вилки, ложки. Из металлов и их сплавов делают станки, самолёты, автомобили, тепловозы, инструменты. Без металлов невозможна современная цивилизация, так как электрические провода также делают из металлов — Cu и Al. Только металлы годятся для получения антенн для радио- и телеприёмников, из металлов делают и лучшие зеркала. При этом чаще используют не чистые металлы, а их смеси (твёрдые растворы) — СПЛАВЫ.
Дефекты в кристаллах
В кристаллах всегда есть дефекты строения, вызванные нарушением расположения атомов кристаллической решетки. Дефекты кристаллического строения разделяют на точечные, линейные и поверхностные.
Причиной образования дефектов являются вакансии (место, где находился атом, обладающий большей энергией и перешедший с одного места на другое). На это место вакансии через некоторое время перемещается один из атомов соседнего слоя и т.д. Таким образом, вакансия перемещается вглубь кристалла. С повышением температуры число вакансий увеличивается, и они чаще перемещаются из одного узла в другой. К точечным дефектам относят также атом, внедренный в междоузлие кристаллической решетки, и замещенный атом, когда место атома одного металла замещается в кристаллической решетке другим, чужеродным атомом. Точечные дефекты вызывают местное искажение кристаллической решетки. Линейные дефекты являются другим важнейшим видом несовершенства кристаллической решетки, когда в результате сдвига на одно межатомное расстояние одной части решетки относительно другой вдоль какой-либо плоскости число рядов атомов в верхней части решетки на один больше, чем в нижней. В данном случае в верхней части решетки появилась как бы лишняя атомная плоскость (экстраплоскость). Край экстраплоскости, перпендикулярный направлению сдвига, называется краевой (линейной) дислокацией, длина которой может достигать многих тысяч межатомных расстояний. Кристаллическая решетка в зоне дислокаций упруго искажена, поскольку атомы в этой зоне смещены относительно их равновесного состояния.
Поверхностные дефекты представляют собой границы раздела между отдельными кристаллами. На границе раздела атомы кристалла расположены не так упорядочено, как в его объеме. Кроме того, по границам раздела скапливаются дислокации и вакансии, а также концентрируются примеси, что еще больше нарушает порядок расположения атомов. При этом сами кристаллы разориентированы, т.е. могут быть повернуты относительно друг друга на десятки градусов.
Дефекты в кристаллах существенно влияют на свойства металлов. Для получения металлов и сплавов высокого качества необходимо свести все дефекты к минимуму. Этого можно добиться, прибегнув к специальным методам обработки, например, к методам термической обработки.
структура
Свойства тугоплавких металлов и сплавов
На верхнем изображении изображены некоторые драгоценные камни изумрудов. Подобно этому, многие другие минералы, соли, металлы, сплавы и алмазы имеют кристаллическую структуру; Но какова связь между его порядком и симметрией??
Если к кристаллу, частицы которого можно наблюдать невооруженным глазом, применяются операции симметрии (инвертировать, вращать его под разными углами, отражать его в плоскости и т. Д.), То будет обнаружено, что он остается неповрежденным во всех измерениях пространства.
Противоположное имеет место для аморфного твердого тела, из которого получают различные упорядочения, подвергая его операции симметрии. Кроме того, ему не хватает структурных шаблонов повторения, что демонстрирует случайное распределение его частиц..
Какая самая маленькая единица, которая составляет структурный образец? На верхнем изображении кристаллическое твердое тело симметрично в пространстве, а аморфное не.
Если вы нарисуете некоторые квадраты, которые окружают оранжевые сферы, и примените операции симметрии, вы обнаружите, что они генерируют другие части кристалла..
Предыдущая вещь повторяется с меньшими и меньшими квадратами, пока не будет найдена асимметричная; предшествующий ему по размеру, по определению, элементарная ячейка.
Унитарная ячейка
Унитарная ячейка — это минимальное структурное выражение, которое позволяет полностью воспроизвести кристаллическое твердое вещество. Из этого можно собрать кристалл, двигая его во всех направлениях пространства.
Его можно рассматривать как небольшой ящик (сундук, ведро, контейнер и т. Д.), В котором частицы, представленные сферами, размещаются по схеме заполнения. Размеры и геометрия этого ящика зависят от длины его осей (a, b и c), а также от углов между ними (α, β и γ).
Самая простая из всех элементарных ячеек — это простая кубическая структура (верхнее изображение (1)). При этом центр сфер занимает углы куба, размещая четыре в его основании и четыре на крыше.
При таком расположении сферы едва занимают 52% от общего объема куба, и поскольку природа не терпит вакуума, не так много соединений или элементов, которые принимают эту структуру.
Однако, если сферы расположены в одном и том же кубе таким образом, что он занимает центр (кубический центр на теле, ОЦК), то будет доступна более компактная и эффективная упаковка (2). Сейчас сферы занимают 68% от общего объема..
С другой стороны, в (3) ни одна сфера не занимает центр куба, но центр их граней, и все они занимают до 74% от общего объема (кубический центр на гранях, куб. См).
Таким образом, можно видеть, что для одного и того же куба могут быть получены другие схемы, варьирующие способ упаковки сфер (ионы, молекулы, атомы и т. Д.).
Анизотропия кристаллов
На поведение и свойства кристаллов влияют многие внутренние и внешние факторы. Анизотропией называют неодинаковость физических свойств среды в разных направлениях. Неодинаковостью обладают следующие свойства:
- прочность;
- твердость;
- электрическое сопротивление;
- тепловое расширение.
Причина анизотропии — различие плотности упаковки атомов или молекул в решетке в различных направлениях.
Свойством анизотропности обладают все кристаллы, а аморфные тела (стекло, смола, резина, парафин и др.) изотропны, т.е. имеют одинаковую плотность атомов в различных направлениях.
Анизотропия свойств важна при использовании монокристаллов — одиночных кристаллов, частицы которых расположены единообразно по всему их объему. Монокристаллы имеют правильную кристаллическую огранку (в форме естественных многогранников), анизотропны по механическим, электрическим и другим физическим свойствам. Так, для монокристалла меди предел прочности в изменяется от 120 до 360 МПа в зависимости от направления приложения нагрузки. А монокристалл поваренной соли может разрушиться, если приложить малейшие усилия к одной из его сторон.
Металлы и сплавы, применяемые в технике, обычно имеют поликристаллическую структуру, т.е. состоят из множества мелких и различно ориентированных в пространстве кристаллов, не имеющих правильной кристаллической огранки и называемых кристаллитами (или зернами). В поликристаллах наблюдается анизотропия. Но вследствие разнообразной, беспорядочной ориентировки кристаллографических плоскостей в различных зернах поликристалл может иметь одинаковые или сходные свойства по разным направлениям и не обнаруживать анизотропию (когда размеры зерен значительно меньше размеров поликристалла и количество их весьма велико). Поэтому часто рассматривают поликристаллическое тело как подобное изотропному. Но при более тонких работах со сплавами, имеющими поликристаллическую структуру, необходимо учитывать их анизотропию. Она может быть вызвана изменением внешних условий (температуры, давления и т.д.) или наличием посторонних примесей в материале.
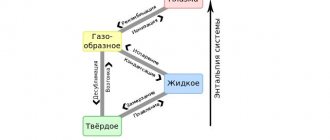
Особенности строения твердых и жидких тел
Состав, строение и свойства металлических сплавов
Перед тем как дать ответ на вопрос о том, что такое плавление, следует рассмотреть особенности строения твердых и жидких тел.
Первые характеризуются наличием постоянной формы, любому изменению которой они оказывают сопротивление. Твердые тела обладают упругостью, отсутствием текучести. Расстояния между частицами, образующими твердое тело, являются небольшими, а силы связи между этими частицами являются значительными в сравнении с таковыми для жидкостей и газов. Силы связи в твердых телах могут иметь различную химическую природу (ван-дер-ваальсовые, металлические, ковалентные, ионные). Существует два способа организации твердых тел:
- кристаллические структуры, когда атомы или молекулы тела расположены в определенных позициях в пространстве, например, металлы;
- аморфные структуры, в которых атомы или молекулы расположены хаотичным способом, например, стекло.
В жидкостях атомы и молекулы расположены дальше друг от друга, чем в твердых телах, поэтому они слабее связаны. Жидкость сохраняет объем при данных условиях, но не сохраняет форму и обладает хорошей текучестью. Частицы жидкости расположены хаотично относительно друг друга.
Следует отметить важный момент, атомы или молекулы в твердом теле находятся в определенных положениях, которые они очень медленно изменяют (например, в процессах диффузии), а вот частицы жидкости постоянно перескакивают из одного положения в другое.
Кристаллизация металлов
Переход из жидкого состояния в твердое (кристаллическое) называют кристаллизацией.
Процессы кристаллизации зависят от температуры и протекают во времени, поэтому кривые охлаждения строятся в координатах «температура — время» (рис. 1).
Рис. 1
Идеальный процесс кристаллизации металла без переохлаждения протекает при температуре TS. При достижении идеальной температуры затвердевания ТS падение температуры прекращается. Каждый чистый металл кристаллизуется при строго индивидуальной постоянной температуре. Чем чище жидкий металл, тем он более склонен к переохлаждению. При увеличении скорости охлаждения степень переохлаждения возрастает, а зерна металла становятся мельче, что улучшает его качество. Для большинства металлов степень переохлаждения при кристаллизации в производственных условиях составляет от 10 до 30°С.
Процесс кристаллизации протекает в две стадии:
- зарождение кристаллов (зародышей, или центров кристаллизации);
- рост кристаллов из центров.
При переохлаждении сплава ниже температуры ТN на многих участках жидкого металла образуются кристаллические зародыши:
- образовавшиеся кристаллы растут свободно и имеют правильную геометрическую форму;
- при соприкосновении растущих кристаллов их правильная форма нарушается, так как в этих участках рост граней прекращается;
- рост кристалла продолжается в тех направлениях, где есть свободный доступ жидкого металла;
- кристаллы, имевшие сначала геометрически правильную форму, после затвердевания приобретают неправильную форму (их называют кристаллитами, или зернами).
Величина зерен, образующихся при кристаллизации, зависит не только от количества самопроизвольно зарождающихся центров кристаллизации, но также и от количества нерастворимых примесей, всегда имеющихся в жидком металле. Они являются центрами кристаллизации. Кристаллическая решетка таких твердых частиц должна быть близка по строению и параметрам решетки кристаллизующегося металла. На образование центров кристаллизации влияет и скорость охлаждения.
Электронное строение металлов и их особенности
Внутреннее строение реальных металлов определяет их физико-химические параметры.
Кристаллическая решетка металлов
Все металлы в твердом фазовом состоянии имеют кристаллическое строение. Это пространственное образование из многократно повторяющихся первичных структур называют кристаллической решеткой. схема кристаллической решетки.
Кристаллическое строение металлов
Кристаллическое строение металлов и сплавов может быть двух типов:
- Межатомная дистанция равна по всем направлениям. Это так называемое изотропное строение. При этом физические свойства кристалла также одинаковы по всем направлениям.
- Межатомное расстояние по горизонтали и по вертикали разное. Такой кристалл называют анизотропным, его параметры зависят от направления.
В реальном куске металлов, который состоит из множества кристаллических фрагментов, атомно кристаллическое строение принадлежит к третьему типу — квазиизотропному. Усредненные параметры такого куска близки к изотропным.
Строение механического слитка
Форма растущих кристаллов определяется:
- условиями их касания друг с другом;
- составом сплава;
- наличием примесей;
- режимом охлаждения.
Механизм образования кристаллов носит дендритный (древовидный) характер. Дендритная кристаллизация характеризуется тем, что рост зародышей происходит с неравномерной скоростью. После образования зародышей их развитие идет в тех плоскостях и направлениях решетки, которые имеют наибольшую плотность упаковки атомов и минимальное расстояние между ними. В этих направлениях образуются длинные ветви будущего кристалла — оси первого порядка. От осей первого порядка начинают расти новые оси — второго порядка, от осей второго порядка — оси третьего порядка и т.д.
Стальные слитки получают охлаждением в металлических формах (изложницах) или на установках непрерывной разливки. В изложнице сталь не может затвердеть одновременно во всем объеме, так как невозможно создать равномерную скорость отвода тепла. Поэтому процесс кристаллизации стали начинается у холодных стенок и дна изложницы и распространяется внутрь жидкого металла. При соприкосновении жидкого металла со стенками изложницы в начальный момент образуется зона мелких равноосных кристаллов. Поскольку объем твердого металла меньше жидкого, между стенкой изложницы и застывшим металлом образуется воздушная прослойка и сама стенка нагревается от соприкосновения с металлом, поэтому скорость охлаждения металла снижается, и кристаллы растут в направлении отвода теплоты. При этом образуется зона, состоящая из древовидных (столбчатых) кристаллов.
Во внутренней зоне слитка в результате замедленного охлаждения образуются равноосные, неориентированные кристаллы больших размеров. В верхней части слитка, которая затвердевает в последнюю очередь, образуется усадочная раковина, так как при охлаждении объем металла уменьшается. Под усадочной раковиной металл получается рыхлым из-за большого количества усадочных пор.
Для получения изделий используют только часть слитка, удаляя усадочную раковину и рыхлый металл слитка для последующего переплава.
Методы изучения строения металлов
Изучение строения металлов и сплавов производится методами макро— и микроанализа, рентгеновским методом, а также методами дефектоскопии (рентгеновской, магнитной, ультразвуковой).
Методом макроанализа изучается макроструктура, т.е. структура, видимая невооруженным глазом или с помощью лупы. При этом выявляются крупные дефекты: трещины, усадочные раковины, газовые пузыри и иное, а также неравномерность распределения примесей в металле. Макроструктуру определяют по изломам металла, по макрошлифам (это образец металла или сплава, одна из сторон которого отшлифована, тщательно обезжирена, протравлена и рассматривается с помощью лупы с увеличением в 5–10 раз).
Микроанализ выявляет структуру металла или сплава по микрошлифам, дополнительно отполированным до зеркального блеска. Шлифы рассматривают в отраженном свете под оптическим микроскопом при увеличении до 3000 раз. Из-за различной ориентировки зерен металла они травятся не в одинаковой степени, и под микроскопом свет также отражается неодинаково. Границы зерен благодаря примесям травятся сильнее, чем основной металл, и выявляются более рельефно. Зная микроструктуру, можно объяснить причины изменения свойств металла.
С помощью рентгеновского анализа изучают атомную структуру металлов, типы и параметры кристаллических решеток, а также дефекты, лежащие в глубине. Этот анализ, основанный на дифракции (отражении) рентгеновских лучей рядами атомов кристаллической решетки, позволяет обнаружить дефекты, не разрушая металла. Вместах дефектов рентгеновские лучи поглощаются меньше, чем в сплошном металле, и поэтому на фотопленке такие лучи образуют темные пятна, соответствующие форме дефекта.
Магнитным методом исследуют дефекты в магнитных металлах (сталь, никель и др.) на глубине до 2 мм. Для этого испытываемое изделие намагничивают, покрывают его поверхность порошком железа, осматривают поверхность и размагничивают изделие. Вокруг дефекта образуется неоднородное поле, и магнитный порошок повторяет очертания дефекта. Ультразвуковым методом осуществляется эффективный контроль качества металла изделий и заготовок практически любых размеров. В импульсных ультразвуковых дефектоскопах ультразвуковая волна от щупа-излучателя распространяется в контролируемом изделии и при встрече с дефектом отражается от него. При этом отраженные волны принимаются, усиливаются и передаются на показывающий индикатор.
Строение и структура металлов
ГЛАВА 7
МЕТАЛЛЫ В СТРОИТЕЛЬСТВЕ
Общие сведения о металлах. Классификация металлов
Металлы (от лат. metallum — шахта, рудник) — группа элементов, в виде простых веществ обладающих характерными металлическими свойствами, такими как высокие тепло- и электропроводность, положительный температурный коэффициент сопротивления, высокая пластичность и металлический блеск.
Большая часть металлов присутствует в природе в виде руд и соединений. Они образуют оксиды, сульфиды, карбонаты и другие химические соединения. Для получения чистых металлов и дальнейшего их применения необходимо выделить их из руд и провести очистку. При необходимости проводят легирование и другую обработку металлов. Изучением этого занимается наука металлургия. Металлургия различает руды чёрных металлов (на основе железа) и цветных (в их состав не входит железо, всего около 70 элементов).
Все металлы и сплавы подразделяются на две группы: черные металлы и цветные.
Черные металлы представляют собой сплав железа с небольшим количеством углерода. Наряду с углеродом черные металлы могут содержать кремний, марганец, фосфор, серу и другие химические элементы, попадающие в металлы из руд или добавляемые в них в процессе плавки. Для улучшения качества или придания специфических свойств в состав черных металлов вводят легирующие добавки — медь, никель, хром, кремний.
В зависимости от содержания углерода черные металлы подразделяются на чугуны и стали.
В сталях содержится до 2% углерода, а в чугунах содержится от 2 до 6,7% углерода.
Цветные металлы представляют собой сплавы на основе алюминия, магния, меди, никеля, хрома, цинка, олова, свинца.
Металлы состоят из зерен, тесно прилегающих друг к другу. Эти зерна можно заметить на свежем изломе металлического стержня невооруженным глазом. Более четко структура металла видна под микроскопом при сильном увеличении.
В зависимости от химического состава структурные составляющие железоуглеродистых сплавов носят следующие наименования:
— аустенит
— твердый раствор углерода в гамма-железе (гамма-железо — одна из форм кристаллов чистого железа); предельная концентрация углерода в аустените 1,7%; аустенит немагнитен, характеризуется большой вязкостью, хорошей сопротивляемостью истиранию и химической стойкостью;
— феррит
— технически чистое железо, которое характеризуется малой твердостью, небольшой прочностью и высокой пластичностью; феррит магнитен; свойства феррита в значительной степени зависят от размера его зерна; в структуре стали феррит располагается в виде отдельных светлых зерен, перемежающихся с темными участками перлита, или в виде светлых окаймлений вокруг зёрен перлита;
— цементит
— химическое соединение железа с углеродом; обладает высокой твердостью, но в, то, же время хрупок; форма цементита в стали оказывает влияние на ее механические свойства, особенно на ударную вязкость;
— перлит
— смесь цементита и феррита; содержание углерода в перлите 0,83 %’, чем мельче зерна перлита в металле, тем выше его механические свойства.
Химический состав и структура металла предопределяет его физические и механические свойства: прочность, твердость, плотность. Механические свойства в значительной степени позволяют определить, насколько хорошо будет работать деталь в эксплуатационных условиях.
Строение и структура металлов
Металлы относятся к твердым телам кристаллического строения.
Твердое тело —это агрегатное состояние вещества, характеризующееся стабильностью формы и объема.По своему внутреннему строению твердые тела разделяются на кристаллические и аморфные.
Кристаллы — это твёрдые тела, частицы которых располагаются в строгом порядке, образуя пространственные периодически повторяющиеся структуры.
Точнее, частицы колеблются около определенных положений равновесия. Если их мысленно соединить прямыми линиями, то получается своего рода «скелет» кристалла. Такое изображение кристалла называется кристаллической решеткой.
Теоретически доказано, что всего может существовать 230 различных пространственных кристаллических структур.
Большинство из них (но не все) обнаружены в природе или созданы искусственно.
Рис. 7.1. Виды кристаллического строения металлов
На рис. 7.1. приведены примеры простых кристаллических решеток: 1 – простая кубическая решетка; 2 – гранецентрированная кубическая решетка; 3 – объемно-центрированная кубическая решетка; 4 – гексагональная решетка.
Металлы имеют относительно сложные типы кубических решеток — объемно центрированная (ОЦК) и гранецентрированная (ГЦК) кубические решетки.
Рис. 7.2. Объемно-центрированная кристаллическая решетка
Основу ОЦК-решетки составляет элементарная кубическая ячейка (рис.7.2.), в которой положительно заряженные ионы металла находятся в вершинах куба, и еще один атом в центре его объема, т. е. на пересечении его диагоналей. Такой тип решетки в определенных диапазонах температур имеют железо, хром, ванадий, вольфрам, молибден и др. металлы.
Рис.7.3. Гранецентрированная кристаллическая решетка
В гранецентрированной кристаллической решетке (ГЦК-решетки) (рис.7.3) элементарной ячейкой служит куб с центрированными гранями. Подобную решетку имеют железо, алюминий, медь, никель, свинец и др. металлы.
Рис.7.4. Гексагональная плотноупакованная кристаллическая решетка
Третьей распространенной разновидностью плотноупакованных решеток является гексагональная плотноупакованная (ГПУ, рис.7.4). ГПУ-ячейка состоит из отстоящих друг от друга на параметр с параллельных центрированных гексагональных оснований. Три иона (атома) находятся на средней плоскости между основаниями.
В гексагональных решетках отношение параметра с/а всегда больше единицы. Такую решетку имеют магний, цинк, кадмий, бериллий, титан и др.
Компактность кристаллической решетки или степень заполненности ее объема атомами является важной характеристикой. Она определяется такими показателями, как параметр решетки, число атомов в каждой элементарной ячейке, координационное число и плотность упаковки.
Параметр решетки – это расстояние между атомами по ребру элементарной ячейки. Параметры решетки измеряются в нанометрах (1 нм = 10-9 м = 10 Å). Параметры кубических решеток характеризуются длиной ребра куба и обозначаются буквой а.
Для характеристики гексагональной решетки принимают два параметра – сторону шестигранника а и высоту призмы с. Когда отношение с/а = 1,633, то атомы упакованы наиболее плотно, и решетка называется гексагональной плотноупакованной (рис. 7.4). Некоторые металлы имеют гексагональную решетку с менее плотной упаковкой атомов (с/а > 1,633). Например, для цинка с/а = 1,86, для кадмия с/а = 1,88.
Параметры, а кубических решеток металлов находятся в пределах от 0,286 до 0,607 нм. Для металлов с гексагональной решеткой, а лежит в пределах 0,228-0,398 нм, а с в пределах 0,357- 0,652 нм.
Параметры кристаллических решеток металлов могут быть измерены с помощью рентгеноструктурного анализа.
При подсчете числа атомов в каждой элементарной ячейке следует иметь в виду, что каждый атом входит одновременно в несколько ячеек. Например, для ГЦК-решетки, каждый атом, находящийся в вершине куба, принадлежит 8 ячейкам, а атом, центрирующий грань, двум. И лишь атом, находящийся в центре куба, полностью принадлежит данной ячейке.
Таким образом, ОЦК — и ГЦК-ячейки содержат соответственно 2 и 4 атома.
Под координационным числом понимается количество ближайших соседей данного атома.
Физические и химические свойства металлов
К физическим свойствам металлов относят цвет, плотность, температуру плавления, теплопроводность, тепловое расширение, теплоемкость, электропроводность, магнитные свойства и др.
Цветом называют способность металлов отражать световое излучение с определенной длиной волны. Например, медь имеет розово-красный цвет, алюминий — серебристо-белый. Плотность металла характеризуется его массой, заключенной в единице объема. По плотности все металлы делят на легкие (менее 4500 кг/м3) и тяжелые. Плотность имеет большое значение при создании различных изделий. Например, в самолетои ракетостроении стремятся использовать более легкие металлы и сплавы (алюминиевые, магниевые, титановые), что способствует снижению массы изделий.
Температурой плавления называют температуру, при которой металл переходит из твердого состояния в жидкое. По температуре плавления различают тугоплавкие металлы (вольфрам — 3416°С, тантал — 2950°С, титан —1725°С и др.) и легкоплавкие (олово — 232°С, свинец — 327°С, цинк — 419,5°С, алюминий — 660°С). Температура плавления имеет большое значение при выборе металлов для изготовления литых изделий, сварных и паяных соединений, термоэлектрических приборов и других изделий. В единицах СИ температуру плавления выражают в градусах Кельвина (К).
Теплопроводностью называют способность металлов передавать тепло от более нагретых к менее нагретым участкам тела. Большой теплопроводностью обладают серебро, медь, алюминий. Железо имеет теплопроводность примерно в три раза меньше, чем алюминий, и в пять раз меньше, чем медь. В единицах СИ теплопроводность имеет размерность Вт/ (м·К).
Тепловым расширением называют способность металлов увеличиваться в размерах при нагревании и уменьшаться — при охлаждении. Тепловое расширение характеризуется коэффициентом линейного расширения
где l1 и l2 — длины тела при температурах t1 и t2. Коэффициент объемного расширения равен 3. Тепловые расширения должны учитываться при сварке, ковке и горячей объемной штамповке, изготовлении литейных форм, штампов, прокатных валков, калибров, выполнении точных соединений и сборке приборов, укладке железнодорожных рельсов.
Теплоемкостью называют способность металла при нагревании поглощать определенное количество тепла. В единицах СИ она имеет размерность Дж/К. Теплоемкость различных металлов сравнивают по величине удельной теплоемкости — количеству тепла, выраженному в больших калориях, которое требуется для повышения температуры 1 кг металла на 1°С (в единицах СИ — Дж/(кг·К).
Способность металлов проводить электрический ток оценивают двумя взаимно противоположными характеристиками — электропроводностью и электросопротивлением. Электрическая проводимость оценивается в СИ в сименсах (См), а удельная электропроводность — в См/м, аналогично электросопротивление выражают в омах (Ом), а удельное электросопротивление — в Ом·м. Хорошая электропроводность необходима, например, для токонесущих проводов (из меди, алюминия). При изготовлении электронагревательных приборов и печей необходимы сплавы с высоким электросопротивлением (из нихрома, константана, манганина). С повышением температуры металла его электропроводность уменьшается, а с понижением — увеличивается.
Магнитные свойства характеризуются абсолютной магнитной проницаемостью или магнитной постоянной, т.е. способностью металлов намагничиваться. В единицах СИ магнитная постоянная имеет размерность Гн/м. Высокими магнитными свойствами обладают железо, никель, кобальт и их сплавы, называемые ферромагнитными. Материалы с магнитными свойствами применяют в электротехнической аппаратуре и для изготовления магнитов.
Химические свойства характеризуют способность металлов и сплавов сопротивляться окислению или вступать в соединение с различными веществами: кислородом воздуха, растворами кислот, растворами щелочей и др.
Чем легче металл вступает в соединение с другими элементами, тем быстрее он разрушается. Химическое разрушение металлов под действием на их поверхность внешней агрессивной среды называют коррозией. Металлы, стойкие к окислению при сильном нагреве, называют жаростойкими или окалиностойкими. Такие металлы применяют для изготовления деталей, которые эксплуатируются в зоне высоких температур.
Сопротивление металлов коррозии, окалинообразованию и растворению определяют по изменению массы испытываемых образцов на единицу поверхности за единицу времени. Химические свойства металлов обязательно учитываются при изготовлении изделий. Особенно это относится к изделиям или деталям, работающим в химически агрессивных средах:
- емкостям для перевозки химических реактивов;
- трубопроводам химических веществ;
- приборам и инструментам в химической промышленности и др.
Химические свойства
Металлы являются восстановителями и вступают в реакцию с неметаллами, образуя оксиды, гидроксиды, соли. Самыми активными являются щелочные и щелочноземельные металлы, расположенные в I и II группах таблицы Менделеева. Благородные металлы (Au, Ag, Pt) малоактивны и не взаимодействуют с кислородом и водой.
Рис. 2. Шкала активности металлов.
Особенности химического взаимодействия металлов с другими элементами описаны в таблице.
| Взаимодействие | Продукты | Уравнение |
| С кислородом | Оксиды | 2Mg + O2 → 2MgO |
| С серой | Сульфиды | Zn + S → ZnS |
| С азотом | Нитриды | 6Li + N2 → 2Li3N |
| С фосфором | Фосфиды | 3Ca + 2P → Ca3P2 |
| С галогенами | Галогениды | 2Na + Cl2 → 2NaCl |
| С водой | Гидроксиды | 2Na + 2H2O → 2NaOH + H2 |
| С кислотами | Соли | 2Al + 3H2SO4 → Al2(SO4)3 + 3H2 |
| С солями (замещают менее активные металлы) | Соль | 2Fe + Cu2SO4 → Fe2SO4 + 2Cu |
Золото растворяется в царской водке (смеси соляной и азотной кислот), серебро – в концентрированной азотной и горячей серной кислотах.
Рис. 3. Золото.
Основные механические свойства металлов
Способность металла сопротивляться воздействию внешних сил характеризуется механическими свойствами: прочностью, упругостью, пластичностью, ударной вязкостью, твердостью и выносливостью. Эти свойства определяют по результатам механических испытаний, когда металлы подвергают воздействию внешних сил (нагрузок). Внешние силы могут быть статическими, динамическими или циклическими (повторно-переменными).
Нагрузка вызывает в твердом теле напряжение и деформацию. Напряжение — величина нагрузки, отнесенная к единице площади поперечного сечения испытываемого образца. Деформация — изменение формы и размеров твердого тела под влиянием приложенных внешних сил. Различают деформации растяжения (сжатия), изгиба, кручения, среза. Материал может подвергаться одному или нескольким видам деформации одновременно.
Для определения прочности, упругости и пластичности металлы в виде образцов круглой или плоской формы испытывают на статическое растяжение (ГОСТ 1497–84). Испытания проводят на разрывных машинах. В результате испытаний получают диаграмму растяжения. По оси абсцисс этой диаграммы откладывают значения деформации, а по оси ординат — нагрузки, приложенные к образцу.
Прочность — способность материала сопротивляться разрушению под действием нагрузок; оцениваемая пределом прочности и пределом текучести. Важным показателем прочности материала является также удельная прочность — отношение предела прочности материала к его плотности. Предел прочности в (временное сопротивление) — это условное напряжение в Па (Н/м2), соответствующее наибольшей нагрузке, предшествующей разрушению образца:
где Рmax— наибольшая нагрузка, Н; F0 — начальная площадь поперечного сечения рабочей части образца, м2.
Истинное сопротивление разрыву Sк — это напряжение, определяемое отношением нагрузки Pк в момент разрыва к площади минимального поперечного сечения образца после разрыва:
Предел текучести (физический) σт — это наименьшее напряжение (в мегапаскалях), при котором образец деформируется без заметного увеличения нагрузки:
где Pт — нагрузка, при которой наблюдается площадка текучести, Н. Площадку текучести имеют, в основном, только малоуглеродистая сталь и латунь. Другие сплавы площадки текучести не имеют.
Состав, структура и свойства металлов
В твердом состоянии все металлы,металлические сплавыобладают кристаллическим строениемсо строго определенным расположением атомов, образующих правильную кристаллическую решетку. Такое упорядоченное расположение атомов отличает кристаллические материалы от аморфных (стекло), в которых атомы расположены беспорядочно. Число атомов в различных сечениях кристаллической решетки неодинаково, поэтому механические, электрические и другие свойства металлов в разных направлениях различны. Это явление называют анизотропией, а материалы – анизотропными.
Металлы, используемые в технике, состоят из большого числа кристаллов правильной и неправильной формы, которые называют зернами или кристаллитами. В 1 см3 металлических изделий (например, стального проката) содержатся десятки тысяч кристаллитов. По границам между зернами металла нарушается правильность строения кристаллической решетки. Кроме того, даже в химически чистом металле содержатся примеси инородных атомов, которые искажают кристаллическую решетку. Все эти нарушения строения приводят, прежде всего, к значительному снижению реальной прочности. Например, теоретическая прочность железа равна 1400 МПа, в то время как практическая не превышает 300 МПа.
Металлы способны при нагревании, приводящем к разрушению кристаллической решетки, переходить в вязкопластичное состояние, а при охлаждении расплава – в кристаллическое. Такой переход происходит при строго определенной температуре, которую называют температурой плавления или кристаллизации. Некоторые металлы (железо, олово и др.) способны при повышении температуры изменять форму и расположение кристаллов в твердом состоянии. Существование одного и того же металла в нескольких кристаллических формах с различным расположением атомов в решетке называется аллотропией.Ряд металлов способны образовывать сплавы– сложные по составу соединения, образовавшиеся в результате взаимодействия двух или нескольких металлов либо металлов с некоторыми неметаллами. В строительстве наибольшее применение нашли сплавы меди, алюминия, а также чугун, сталь, представляющие собой соединения железа и углерода.
Свойства металлов и сплавов зависят от их состава и микроструктуры. Впервые эту зависимость, которую широко используют на практике, установил академик Н.С. Курнаков (1880 – 1941). Как правило, чем выше температура плавления металла или сплава, тем больше его прочность, лучше тепло- и электропроводность. Для получения сплавов с заданными свойствами, а также оценки надежности работы металлических конструкций применяют макроскопический и микроскопический анализы: макроскопический проводят невооруженным глазом или используют лупу с увеличением до 30 раз на специально подготовленных образцах; микроскопический анализ заключается в исследовании структуры и состава металлов и сплавов при помощи специальных оптических и электронных микроскопов, где увеличение может достигать 3000 раз и более.
Механические свойстваметаллов зависят от вида нагрузки, условий ее действия, температуры окружающей среды. Прочностные характеристики определяют испытанием стандартных образцов или самих изделий на специальных машинах. Режим испытания может быть статическим – нагрузка на образец увеличивается постепенно (определение прочности на сжатие, изгиб, разрыв), динамическим – нагрузка на образец действует мгновенно (испытание на удар), и повторно-переменным – нагрузка на образец многократно изменяется по величине и направлению (испытание на усталость). Металлы испытывают на растяжение, сжатие, кручение, удар, усталость, твердость, ползучесть при комнатной, низких и высоких температурах.
Испытание на растяжениепроводят с использованием разрывных машин. По величинам растягивающих нагрузок и соответствующим удлинениям образца вычерчивают диаграмму растяжения, характеризующую поведение металла или сплава под нагрузкой до момента разрушения. Для испытания на удариспользуют маятниковый копер, которыйпозволяет определить способность металла противодействовать динамическим нагрузкам и выявить его склонность к хрупкому разрушению при различных температурах. Испытанием на усталостьоценивают возможность работы металлов (сплава) при действии многократных нагрузок, изменяющихся по величине и знаку. Способность металлов выдерживать большое число циклов испытаний называют выносливостью.Испытания проводят на цилиндрических образцах путем воздействия на них при вращении изгибающих нагрузок, которые вызывают знакопеременные напряжения, и доводят образец до разрушения.
Для определения твердостина практике применяют различные способы, основанные на внедрении в металлическую поверхность наконечника, выполненного из особо твердого материала (закаленная сталь, алмаз, сапфир) и имеющего правильную форму в виде шарика, конуса или пирамиды. Наибольшее распространение получил метод Бринелля, основанный на расчете твердости по диаметру отпечатка вдавливаемого в поверхность металлического шарика определенной массы и диаметра. Условия испытания ограничивают величину и время действия прилагаемой нагрузки.
При изучении свойств металлов (сплавов) большое внимание уделяют исследованию процессов их разрушения при действии газообразных и жидких сред в условиях обычной и высоких температур. Важность этих работ подчеркивает тот факт, что ежегодно 30 % производимого металла идет на восстановление потерь от коррозии, из них 10 % теряется безвозвратно.
Коррозияначинается с поверхности металла и распространяется вглубь. Интенсивность коррозионного разрушения зависит в основном от трех факторов: первый – химический состав и микроструктура металла или сплава; второй – химический состав окружающей среды и процентное содержание в ней агрессивных веществ (кислорода, кислот, щелочей); третий – температура окружающей среды. В зависимости от причин, вызывающих разрушение, коррозия может быть химической и электрохимической.
Поверхностное разрушение металла под действием газов при высокой температуре или органических жидкостей (спирта, бензина, нефти, мазута и т.п.) называют химической коррозией.Примером химической коррозии является процесс окисления при высоких температурах металлической арматуры печей, клапанов двигателей внутреннего сгорания, лопаток газовых турбин.
Электрохимическая коррозияметаллических изделий происходит в различных водных растворах, проводящих электрический ток. Это наиболее распространенный вид коррозии. Она наблюдается в атмосферных условиях, на море, в земле, грунтовых водах, в растворах различных кислот и солей. Значительная часть строительных металлических конструкций и изделий (каркасы и крыши зданий, фермы мостов, арматура в железобетоне) подвержена электрохимической коррозии. Сущность процесса электрохимической коррозии заключается в том, что атомы, находящиеся в узлах кристаллической решетки, при контакте с электролитом переходят в раствор в форме ионов, вызывая разрушение металла.
Существует несколько видов коррозионных разрушений: равномерное,протекающее по всей поверхности с одинаковой скоростью; неравномерное– сплошное, скорость которого на отдельных участках зависитот структуры сплава и наличия дефектов на поверхности изделий; местноеили локальное,наблюдаемое на отдельных участках поверхности металла (сплава).
Одним из способов предотвращения коррозии является ликвидация вызывающих ее условий: неоднородность строения, наличие дефектов на поверхности изделий, неравномерность освещенности и теплового нагрева. Кроме того, для борьбы с коррозией применяют специальные методы защиты: введение в состав легирующих добавок, электрохимическая защита (анодная или катодная), обработка коррозионной среды и защитные покрытия. Защитные действия легирующих добавок–Си, А1, Тi, V, Сr, Ni, Со и др., которые вводят для изменения структуры и свойств металлов, обусловлены или образованием на поверхности изделий коррозионностойких оксидных пленок, или созданием сплавов, обладающих высокой стойкостью к агрессивным средам.
Для надежной и долговечной защиты металлических конструкций, стальных закладных деталей, используемых при производстве сборного железобетона, все чаще применяют металлические покрытия,которые наносятгальваническимигорячим способами, металлизацией, плакированием. При гальваническом способепутем электролитического осаждения из раствора солей создается тонкий защитный слой какого-либо металла на поверхности изделия. В качестве примера можно привести оцинкование закладных деталей для железобетонных конструкций. При горячем способеизделия погружают в ванну с расплавленным защитным металлом (цинк, олово, свинец). Металлизацияявляется распространенным способом защиты в строительстве. Она состоит в нанесении сжатым воздухом тончайшего слоя распыленного расплавленного металла (цинк, алюминий) на поверхность защищаемого от коррозии металлического изделия или конструкции. Еще одним вариантом защиты металлических покрытий от коррозии является плакирование.
Плакирование– термомеханический метод получения двух- и многослойных металлов (биметаллов), прочно соединенных между собой по всей плоскости соприкосновения. Металлургическими заводами организовано производство листа, проволоки, труб, покрытых цинком, алюминием, кремнием.
Защиту от коррозии несущих и ограждающих металлоконструкций в условиях строительно-монтажной площадки производят лакокрасочными составамина основе битумов, полимеров и других материалов. Это направление является приоритетным в настоящее время, так как при наименьших энергозатратах можно получить надежное долговечное покрытие. К применяемым составам относятся цинкосодержащие, термореактивные краски на основе высокомолекулярных смол (эпоксидных, полиэфирных). Последние наносят на поверхность металлических изделий и конструкций в электрическом поле при помощи пистолета-распылителя с расположенным внутри источником высокого напряжения. Их преимущество заключается в отсутствии токсичных растворителей, возможности применения безотходной технологии нанесения, отсутствии грунтового слоя и высоком качестве оплавленного, плотного покрытия, обладающего повышенной ударной прочностью, коррозионной стойкостью, адгезией к защищаемой поверхности. В зависимости от назначения оно может быть тонкослойным и фактурным, толщиной от менее 1 мкм до 20 мкм и более. Оптимальный вариант защиты выбирают в зависимости от материала конструкции, степени агрессивного воздействия на него и технико-экономической целесообразности. При необходимости обеспечения особенно надежной и долговечной защиты стальных конструкций применяют комбинированные покрытия, например, металлические и лакокрасочные.
Снизить разрушающее действие коррозионной среды на металлы и сплавы можно также путем введения в ее состав специальных добавок – ингибиторов,замедляющих процесс коррозии.
Кразрушающим факторам относится также действие на металлические изделия и конструкции огня. Под действием открытого пламени и высокой температуры металлы размягчаются, деформируются и растрескиваются.
Незащищенные стальные конструкции в зависимости от толщины элементов, сечения и действующих напряжений имеют предел огнестойкости 0,1 – 0,44 часа. При действии огня несущая способность металлических конструкций снижается вследствие уменьшения при нагревании прочности и упругости металла, а также за счет появления пластических, температурных деформаций. Металлы являются несгораемыми материалами, но обладают высокой теплопроводностью, поэтому их огнезащита заключается в создании на поверхности металлических элементов конструкций теплоизолирующих экранов, обеспечивающих высокую сопротивляемость действию огня и высоких температур. Традиционными средствами огнезащитыметаллических конструкций являются тяжелые и легкие бетоны, кирпич, цементно-песчаные штукатурки.Эти материалы могут создать практически любой предел огнестойкости конструкций. Так для обеспечения предела огнестойкости стальной конструкции, равного 2 часам, необходим слой тяжелого бетона или гипса толщиной 60 мм, штукатурки – 50 – 60 мм, кирпича – 65 мм.
В последние годы все большее применение находят теплоизоляционные штукатурки и огнезащитные покрытияна основе глины, жидкого стекла, гипса с использованием в качестве огнестойких заполнителей и наполнителей вспученного перлита, вермикулита, асбеста и минерального каолинового волокна, обладающих высокими теплоизоляционными свойствами. Составы наносят на поверхность металлоконструкций пистолетом-распылителем. В зависимости от требуемой огнезащиты (45 – 150 мин) и толщины металла в конструкции толщина защитного слоя составляет от 8 до 40 мм.
Одним из перспективных средств огнезащитыявляются вспучивающиеся краски,состоящие, например, из растворителя, акрилового полимера и пенообразующего антипирена, которые наносят на поверхность металлоконструкций тонким слоем (1 – 1,2 мм). При температуре около 170 °С краска вспучивается, образуя пористый термоизоляционный слой, толщина которого составляет несколько сантиметров. Благодаря низкой теплопроводности вспененная масса предотвращает быстрый нагрев металла, увеличивая огнестойкость до 1 часа. Кроме того, для огнезащиты металлических конструкций используют плитные и листовые теплоизоляционные материалыв виде асбестоцементных и асбестогипсовых облицовочных плит, гипсокартонных и гипсоволокнистых листов.
Как показала практика эксплуатации, причиной разрушения металлических конструкций может быть также накопление на их поверхности продуктов жизнедеятельности микроорганизмов: органических кислот, сульфидов, сероводорода, аммиака – биологическая коррозия.Длязащитыметаллоконструкций от биоповрежденийиспользуют мастичныеикрасочныесоставы на основе каменноугольной, эпоксидной, поливинилхлоридной смол с введением в состав эффективных биоцидных добавок.
Упругость, пластичность, вязкость
Упругость — способность материала восстанавливать первоначальную форму и размеры после прекращения действия нагрузки Руп, ее оценивают пределом пропорциональности σпц и пределом упругости σуп. Предел пропорциональности σпц — напряжение (МПа), выше которого нарушается пропорциональность между прилагаемым напряжением и деформацией образца:
где F0 — начальная площадь поперечного сечения рабочей части образца, м2; Рпц — нагрузка предела пропорциональности, Н.
Предел упругости (условный) σ0,05 — это условное напряжение в мегапаскалях, соответствующее нагрузке, при которой остаточная деформация впервые достигает 0,05% от расчетной длины образца l0:
где Р0,05 — нагрузка предела упругости, Н.
Пластичность, т.е. способность материала принимать новую форму и размеры под действием внешних сил, не разрушаясь, характеризуется относительным удлинением и относительным сужением. Относительное удлинение (после разрыва) σ — это отношение приращения (lк – l0) расчетной длины образца после разрыва к его первоначальной расчетной длине l0, выраженное в процентах: δ = [(lк – l0) / l0] · 100%. Относительное сужение (после разрыва) ψ — это отношение разности начальной и минимальной площадей (F0 – Fк) поперечного сечения образца после разрыва к начальной площади F0 поперечного сечения, выраженное в процентах: Ψ = [(F0 – Fк)/F0] · 100%. Чем больше значения относительного удлинения и сужения для материала, тем он более пластичен. У хрупких материалов эти значения близки к нулю. Хрупкость конструкционного материала является отрицательным свойством. Для устранения этого свойства металл легируют, или подвергают термической обработке.
Ударная вязкость, т.е. способность материала сопротивляться динамическим нагрузкам, определяется как отношение затраченной на излом образца работы W (в МДж) к площади его поперечного сечения F (в м2) в месте надреза КС = W/F. Для испытания (ГОСТ 9454–78) изготовляют специальные стандартные образцы, имеющие форму квадратных брусочков с надрезом. Испытывают образец на маятниковых копрах. Определение ударной вязкости важно для некоторых металлов, работающих при минусовых температурах и проявляющих склонность к хладноломкости.
Циклическая вязкость — это способность материалов поглощать энергию при повторно-переменных нагрузках. Материалы с высокой циклической вязкостью быстро гасят вибрации, которые часто являются причиной преждевременного разрушения.
Твердость, усталость, выносливость
Твердостью называют способность материала сопротивляться проникновению в него другого, более твердого тела. Высокой твердостью должны обладать металлорежущие инструменты: резцы, сверла, фрезы, а также поверхностноупрочненные детали. Твердость металла определяют способами Бринелля, Роквелла и Виккерса.
За меру твердости НВ принимают отношение нагрузки к площади поверхности отпечатка диаметром d и глубиной t, который образуется при вдавливании силой Р шарика диаметром D. Числовое значение твердости определяют так: измеряют диаметр отпечатка с помощью оптической лупы (с делениями), по полученному значению находят в таблице, приложенной к ГОСТу, соответствующее число твердости. Для оценки твердости металлов в малых объемах, например на зернах металла или его структурных составляющих, применяют способ определения микротвердости.
Усталостью называют процесс постепенного накопления повреждений материала под действием повторно-переменных напряжений, приводящий к образованию трещин и разрушению. Усталость металла обусловлена концентрацией напряжений в отдельных его объемах, в которых имеются неметаллические включения: газовые пузыри, различные местные дефекты и т.д. Характерным является усталостный излом, образующийся после разрушения образца в результате многократного нагружения и состоящий из двух разных по внешнему виду частей. Одна часть излома с ровной (затертой) поверхностью образуется вследствие трения поверхностей в области трещин, возникших от действия повторно-переменных нагрузок, другая часть с зернистым изломом возникает в момент разрушения образца. Испытания на усталость проводят
на специальных машинах. Наиболее распространены машины для повторно-переменного изгибания вращающегося образца, закрепленного одним или обоими концами, а также машины для испытаний на растяжение-сжатие и на повторнопеременное кручение. В результате испытаний определяют предел выносливости, характеризующий сопротивление усталости.
Выносливость — свойство материала противостоять усталости. Предел выносливости — это максимальное напряжение, которое может выдержать металл без разрушения заданное число циклов нагружения. Между пределом выносливости и пределом прочности существует приближенная зависимость
где σ-1 и σ-1р — соответственно пределы выносливости при изгибе и растяжении-сжатии; σв — предел прочности.
Испытания на ударную вязкость, усталостную прочность, ползучесть
Кроме статических испытаний на ударную вязкость, изделия подвергают испытанию под действием ударных (динамических) знакопеременных нагрузок и высоких температур. Для испытаний применяют стандартный надрезанный образец, который устанавливают на опорах копра. Маятник определенной массы поднимают на установленную высоту Н, закрепляют его, а затем освобожденный от защелки маятник падает, разрушает образец и снова поднимается на некоторую высоту h. Такой способ определения ударной вязкости наиболее простой. Для облегчения расчетов пользуются таблицами, в которых для каждого подъема маятника после разрушения образца указана работа удара.
Испытания на усталостную прочность. Усталости подвержены вагонные оси, коленчатые валы, лопатки турбин, рессоры, пружины и др. Тщательное шлифование, полирование
и упрочнение поверхности деталей значительно увеличивают сопротивление усталости и увеличивают срок службы изделия. Испытания на усталостную прочность производят на различных машинах в зависимости от характера работы деталей. Наиболее распространеными машины для испытания: 1) изгибом при вращении; 2) при растяжении-сжатии; 3) при кручении.
Испытания на ползучесть. Многие детали машин работают в условиях воздействия статических нагрузок при повышенных температурах. Это детали паровых и газовых турбин, химической, нефтяной аппаратуры и т.д.
Ползучестью называют свойство металла медленно и непрерывно удлиняться («ползти») под действием приложенных к нему постоянных рабочих напряжений в условиях повышенных и высоких температур. Если у свинца, алюминия и многих сплавов ползучесть наблюдается уже при температуре 20°С, то сталь обнаруживает заметную ползучесть, только начиная с температуры 350–400°С. Количественной характеристикой ползучести является так называемый предел ползучести. Испытания на ползучесть производятся на специальных установках, в которых имеются нагревательные устройства и приборы. Применяются и низкотемпературные установки, которые влияют в первую очередь на прочность и пластичность изделий.
Технологические и эксплуатационные свойства
Технологические свойства характеризуют способность металлов подвергаться обработке в холодном и горячем состояниях. К основным технологическим свойствам относят обрабатываемость резанием, свариваемость, ковкость, литейные свойства и др.
Обрабатываемость резанием — одно из важнейших технологических свойств, потому что подавляющее большинство
заготовок, а также деталей сварных узлов и конструкций подвергается механической обработке. Одни металлы обрабатываются хорошо, до получения чистой и гладкой поверхности, другие же, имеющие высокую твердость, плохо. Улучшить обрабатываемость, например, стали можно термической обработкой, понижая или повышая твердость материала.
Свариваемость — способность металлов образовывать сварное соединение, свойства которого близки к свойствам основного металла. Ее определяют пробой сваренного образца на загиб или растяжение.
Ковкость — способность металла обрабатываться давлением в холодном или горячем состоянии без признаков разрушения. Ее определяют кузнечной пробой на осадку до заданной степени деформации. Если на боковой поверхности образца трещина не образуется, то такой образец считается выдержавшим пробу, испытываемый металл — пригодным для обработки давлением.
Литейные свойства металлов характеризуют способность их образовывать отливки без трещин, раковин и других дефектов. Жидкотекучесть — способность расплавленного металла хорошо заполнять полость литейной формы.
Усадка при кристаллизации — это уменьшение объема металла при переходе из жидкого состояния в твердое; является причиной образования усадочных раковин и усадочной пористости в слитках и отливках. Ликвация — неоднородность химического состава сплавов, возникающая при их кристаллизации. Обусловлена ликвация тем, что сплавы, в отличие от чистых металлов, кристаллизуются не при фиксированной температуре, а в интервале температур.
Эксплуатационные свойства определяют в зависимости от условий работы машины специальными испытаниями. Износостойкость — свойство материала оказывать сопротивление износу, т.е. постепенному изменению размеров и формы тела вследствие разрушения поверхностного слоя изделия при трении. Также к эксплуатационным свойствам относят хладостойкость, жаропрочность, антифрикционность и др.