В природе металлы активно вступают в химические реакции с кислотами, щелочами и атмосферным кислородом. В большинстве случаев для этого не требуется дополнительная обработка (химическая, термическая). При сильном нагреве металлы начинают активно вступать в реакцию с углеродом, что приводит к образованию сложных соединений под названием карбиды. Эти соединения отличаются рядом необычных свойств — высокая прочность, тугоплавкость, химическая инертность. Какие бывают карбиды металлов? Как эти соединения применяются в промышленности? Какие вещества получили наибольшее применение?
Состав и виды карбидов
Карбиды не являются отдельным веществом. Это соединение углерода с металлами и неметаллами. Причем, следует учитывать, что углерод должен обладать большей электроотрицательностью в получаемом веществе по сравнению с другими используемыми элементами. Это дает возможность избежать производства галогенов, оксидов и других углеродных соединений.
На сегодняшний день различают три вида карбида, состав которых отличен друг от друга:
- Ковалентные соединения. К данному виду относят два элемента — кремний и бром. Это соединения с прочной межатомной связью, что обеспечивает высокую температуру плавления и химическую инертность. Окисление веществ данной группы возможно только при их нагреве свыше 1000 градусов Цельсия. Твердость вещества с бромом настолько высока, что способна конкурировать даже с алмазами. Вещество с кремнием менее прочное, но 8 баллов по шкале Мооса имеет. При этом растворить данное вещество возможно только в царской водке или с помощью концентрированной азотной или плавиковой кислоты.
- Ионные соединения или солеобразные. Вещества данной группы образуются с помощью металлов 1 и 2 группы таблицы Менделеева, а также алюминием. Данные соединения характеризуются высокой температурой плавления. Карбиды ионного вида распадаются под воздействием воды и кислот. При протекании реакции выделяется углеводород и остается гидроксид металла.
- Ионно-ковалентно-металлические или металлоподобные соединения. Образуются с помощью металлов с 4 по 8 группу, а также кобальтом, никелем и железом. Отличительная особенность металлоподобных веществ — это высокая прочность и температура плавления. Данный вид соединений делится на два типа:
- Ацетилениды — при гидролизе образуют этин или ацетилен. Карбид кальция относится к данному типу соединений.
- Метаниды — при вступлении в реакцию с водой или разбавленными кислотами образуют метан. Чаще бесцветны. Сюда относят карбид алюминия, магния, бериллия.
Читать также: Сварис 200 схема принципиальная pdf
Что такое карбид. Свойства карбида. Применение карбида
Забава детства. Так многие вспоминают о карбиде, особенно бывшие мальчишки, а ныне, конечно, взрослые мужчины.
Они брали камешки на строительных рынках. Покупать не покупали, а так, таскали с развалов и из кузовов грузовиков.
Добычу клали в бутылки, заливали водой, закрывали, встряхивали. Оставалось кинуть тару и полюбоваться взрывом.
Любовались и белесыми пузырями, которые карбид давал, попадая в лужи. Однако, кому обязаны таким весельем, сорванцы прошлых лет, зачастую не знали.
Что такое карбид? Попробуем ответить на вопрос, кажущийся неважным в детстве.
Что такое карбид
Карбит – не конкретное вещество, а группа соединений элементов с углеродом. Последний должен быть более электроотрицательным, чем «сосед».
Это обязательное условие, исключающее из ряда карбидов галогениды и оксиды углерода.
Под электроотрицательностью понимается способность атома сдвигать к себе электроны других веществ.
Электротрицательность углерода равна 2,6. Это данные шкалы Полинга. Она выстроена с учетом, что ионность в ковалентной связи делает эту связь прочнее.
Получается, электротрицательность вторых элементов в карбидах должна быть меньше 2,6.
Большинство подходящих элементов – металлы. Но, около 15% карбидов их не содержат.
Внешне карбиды – кристаллические, как правило, бесцветные, прозрачные вещества. Блеск у них алмазный.
Им соединения обязаны углероду, который является основой не только карбидов, но и алмазов.
По сути, герои статьи являются бриллиантами, в которых часть атомов замещена другими элементами.
Есть и цветные дуэты с углеродом, к примеру, карбид железа. Это всем знакомый цемент. Окрас у соединения серый.
Получается, свойства карбидов могут разниться. Несовпадения рассмотрим в главе «Виды». Пока же, изучим общие характеристики класса соединений.
Свойства карбида
К общим свойствам карбидов относится твердость. Она может быть больше, или меньше, но всегда выше среднего.
У некоторых представителей группы показатель близок к корунду и алмазу. Это самые твердые минералы на земле.
Особенно отличились карбиды переходных металлов. Это элементы побочных подгрупп периодической системы. У всех переходных металлов есть электроны на d- и f-орбиталях.
Обобщает карбиды и высокая температура плавления. Как правило, она выше, чем у входящего в соединение металла.
Если он из переходных, размягчение может начинаться лишь при 3000 градусов Цельсия.
Интересно, что температура плавления поднимается вместе с номером группы, к коей принадлежит «сосед» углерода.
Наиболее тугоплавкими являются карбиды с элементами из 5-7-ой групп таблицы Менделеева.
Где карбид можно понять по структуре соединений. Их решетки, зачастую, дефектны.
Это значит, есть отклонения от теоретической схемы, разрывы и смещения. Именно поэтому свойства карбидов могут в 100, а то и 1000 раз разниться с высчитанными по формулам.
Так, многие соединения класса устойчивы к коррозии и не растворяются в большинстве кислот.
Виды карбидов
Основных видов карбидов три. Первый – ковалентные соединения. Валентность – предрасположенность к определенному числу химических связей.
Ковалентная связь – это перекрытие валентных облаков разных элементов. То есть, у них образуются общие электронные пары. Именно такие лежат в основе ковалентных карбидов.
К ковалентным относятся карбиды лишь двух элементов: брома и кремния. Оба соединения химически инертны. Их межатомные связи прочны.
В итоге, карбиды группы трудно расплавить, — решетка не хочет рушиться. Прочность связи делает оба соединения твердыми.
Карбид брома даже соперничает с алмазом. Некоторые образцы углеродного соединения царапают бриллианты, то есть, тверже них.
Карбид кремния алмаз не «побеждает», но свои достойные 8 баллов по шкале Мооса имеет.
Растворяют ковалентные карбиды лишь плавиковая кислота, концентрированная азотная и царская водка. Окисление карбидов группы происходит лишь при нагреве до 1000 градусов.
Второй вид карбидов – ионный. Его, так же, именуют солеобразным. Все образованны металлами 1-ой и 2-ой групп таблицы Менделеева.
В класс включен и карбид алюминия. Соединения группы разлагаются не только кислотами, но и водой.
Камешки, заставляющие «закипать» лужи, к примеру, — карбид кальция. Он, кстати, довольно токсичен, может разъесть слизистые. Зачем же его завозят на строительные рынки, поймем в следующей главе.
При реакции ионных карбидов с водой выделяется водород. В жидкости формируется и выпадает в осадок гидроксид металла.
Реакция протекает бурно. Резкий выброс на поверхность воды водорода и дает то самое пузырение.
Третий вид карбидов – ионно-ковалентно-металлические, попросту, металлоподобные.
Такие соединения формируются элементами 4-ой, 5-ой, 6-ой, 7-ой групп периодической системы. Исключения: — карбиды никеля, кобальта и железа.
Если у ковалентных карбидов химическая активность низкая, а у ионных – высокая, то у третьего вида соединений она средняя.
Примечательно строение молекул. Их основа – атомы металла. Атомы же углерода находятся в пустотах между ними.
Поэтому, к примеру, карбид вольфрама называют внедренным. Имеется в виду, что углерод внедрился в кристаллическую решетку металла.
Такое строение обеспечивает рекордную прочность и высокую температуру плавления. Еще одно известное соединение группы – карбид титана.
Применение карбида
Карбид титана стал основой безвольфрамовых, но столь же твердых сплавов.
К тому же, соединение служит покрытием инструментария, в основном, промышленного и строительного.
Такое напыление сводит к минимуму износ деталей и позволяет обрабатывать ими даже самые твердые материалы.
Карбид кремния, так же, используют в качестве абразива. В природном виде, коим является минерал муассанит, соединение цениться ювелирами, причем, выше чем близкий по виду и свойствам фианит.
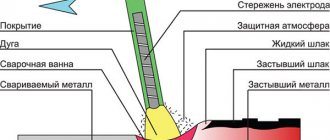
Карбид кальция нужен при сварочных работах. Из соединения получают ацетилен. Карбид служит его источником, а заодно, и топливом для машин кислородной сварки.
Ацетилен – газ. Одного его достаточно для работы аппаратов. Но, есть еще и вода. Карбид кальция вступает с ней в бурную реакцию.
Итог – не только пузырьки, нравящиеся детям, но и обилие тепла – еще одного источника энергии.
Карбид бора применяют в качестве огнеупора. Температура плавления соединения составляет почти 2500 градусов.
Прочность карбида позволяет добавлять его в бронежилеты. Защитить материал способен не только от пуль, но и радиации.
Поэтому, один из ответов на вопрос, где взять карбид бора, — в защитных экранах, задерживающих излучение.
Список карбидов и их роли в жизни общества может занять многие страницы. Соединений несколько десятков и у каждого из них есть применение, причем, не одно. Нет и единственной схемы получения карбидов.
Придется ограничиться общими фразами. Однако, и в них есть толика полезной информации.
Получение карбидов
Большинство карбидов именно получают, а не добывают. Первый синтез проведен в начале 19-го столетия.
Англичанин по фамилии Дэви получил карбид калия. В 1863-ем создали карбид меди.
Он оказался неустойчивым, в отличие от третьего синтезированного соединения углерода с железом.
Смотря на опытные образцы, ученые не могли понять, где найти карбид за пределами лабораторий.
Минералы, в которых металлы соединены с углеродом открыли лишь в начале 20-го века.
Кроме муассанита, геологи нашли когенит – смесь карбида кобальта с никелем и железом.
Судя по дате открытия карбидных минералов, они не являются распространенными.
Поэтому, в промышленных масштабах героев статьи до сих пор синтезируют. Масса карбида может получиться, к примеру, из древесного угля и оксидов металлов.
Они преобразуются в карбиды при помощи вольтовой дуги и электрической печи.
Цена карбида
Карбид кальция купить предлагают примерно за 40-90 рублей за килограмм. Соединение углерода с бором стоит от 100-та рублей за кило.
Купить карбид кремния предлагают примерно по 160 рублей за 1000 граммов.
А вот за кило карбида гафния придется выложить около 21 000 рублей, причем, при оптовых закупках.
То есть, стоимость материала во многом зависит от присутствующего в нем металла, или неметалла. Существует даже карбид золота.
Он, кстати, способен взорваться при простом пересыпании порошка. Так что, даже за большую цену, доставить сырье потребителю – задача не из легких.
Свойства
Благодаря своим свойствам, эти соединения нашли широкое применение в машиностроении, а также в строительстве.
- Высокая твердость материала. У различных соединений она варьируется, но всегда остается выше средней. Они являются самыми твердыми минералами.
- Температура плавления. Практически всегда она выше температуры плавления металла входящего в соединение и может превышать 2000 градусов.
- Устойчивость к коррозии. Многие соединения не вступают в реакцию с различными кислотами и довольно устойчивы к внешним агрессивным факторам.
- Взаимодействие с водой. Практически все карбидные соединения вступают в реакцию с водой, например, при взаимодействии с карбидом кальция можно его взрывать. Условия взаимодействия могут отличаться и зависят от характера связи в соединении.
Качественная реакция
Мало знаний о том, где найти карбид, необходимо удостовериться в подлинности вещества. Для качественной реакции понадобится всего лишь немного воды (на улице можно воспользоваться даже собственной слюной). При взаимодействии CaC2 происходит выделение метана и гидроксида кальция. Можно наблюдать характерное шипение, а если поднести в этот момент спичку — воспламенение.
Из-за бурной реакции с водой карбид разлагается от атмосферной влаги. Поэтому вопрос о том, где найти карбид кальция на улице, весьма спорный. Известно, что в чистом виде его не существует, данное соединение является в большей части искусственным, нежели природным.
Производство карбида
Ковалентные и солеобразные соединения получают простым методом. В электрическую печь помещают смесь из дробленого кокса и оксида металла и нагревают. При высоких температурах оксид элемента вступает в реакцию с коксом. При таком способе часть кокса, которая состоит из углерода, соединяется с атомами элемента, входящими в оксид. В результате образуется требуемый карбид и угарный газ. Готовую расплавленную смесь разливают по специальным формам, а после застывания дробят и сортируют по размеру гранул. Несмотря на простоту данного способа, получение карбида с его помощью является довольно энергозатратным, поскольку требует поддержания высоких температур (1600-2500 градусов) на всем протяжении реакции.
Существуют и альтернативные способы получения некоторых видов веществ. Как правило, это разложение соединения в результате которого и получается требуемый элемент. Формула распада будет отличаться в зависимости от конкретного соединения.
Как выглядит карбид?
Чтобы определить, где найти карбид на улице, нужно знать его физические свойства. Физически вещество является твердым, его цвет может быть темным, имея сероватый или коричневый оттенок. Цвет зависит от количества углерода. Также имеется специфический запах, который характеризует данное вещество.
По консистенции он твердый, но легко крошится, превращаясь в порошок. Если поднести спичку, то начнется горение с выделением углерода и разложением кальция. Правда, этого можно достичь при высоких температурах, например охотничьей спичкой.
Применение в промышленности
Карбид кальция является важным соединением для получения ацетилена, газа, который используется при кислородной сварке и обработке металлов. При горении с кислородом ацетилен способен достигать 3150 градусов Цельсия. Это позволяет работать с тугоплавкими металлами, требующими температуру вдвое большую,чем температура плавления самого металла.
Карбид бора используется как огнеупорный материал, поскольку температура плавления такого соединения выше 2400 градусов. При этом он же встречается в бронежилетах,так как способен защитить не только от пуль и осколков, но и от радиации. Для покрытия промышленного и строительного инструмента используют карбид титана. Его прочность позволяет повысить износостойкость деталей и обрабатывать даже самые прочные материалы.
Читать также: Чертеж цилиндрического зубчатого колеса
Применение
Карбиды применяют в производстве чугунов и сталей, керамики, различных сплавов, как абразивные и шлифующие материалы, как восстановители, раскислители, катализаторы и др. WC и TiC входят в состав твердых сплавов, из которых готовят режущий инструмент; карбид кальция СаС2 используют для получения ацетилена; из карбида кремния SiC (карборунд) готовят шлифовальные круги и другие абразивы; карбид железа Fe3C (цементит) входит в состав чугунов и сталей, из карбида вольфрама и карбида хрома производят порошки, используемые при газотермическом напылении.
Хранение и транспортировка
Поскольку карбид при вступлении в реакцию с влагой приводит к выделению большого количества тепла и взрывоопасного газа ацетилена, хранят данное вещество в герметичных баках или барабанах. Работа с такими баками требует особой осторожности. Газ ацетилен легче воздуха и способен самовоспламеняться, при этом обладает наркотическим действием. При вскрытии барабанов с карбидом используют специальный инструмент, исключающий возникновение искр, а при попадании вещества на кожу требуется немедленно промыть водой пораженный участок и смазать жирным кремом.
Помещения хранения должны хорошо проветриваться, а содержание других веществ по соседству — запрещено. Это может привести к опасным реакциям. Неправильное хранение может как взорвать карбид, так и привести его в негодное состояние.
Срок хранения доходит всего до полугода.
Перевозка осуществляется только крытым транспортом. Воздушная доставка запрещена.
Техника безопасности
Карбид для сварки относится к классу взрывоопасных веществ. Безопасное применение карбида обеспечивается учетом ряда условий:
- Ацетилен является легковоспламеняющимся газом, а сам сухой карбид также взрывоопасен, поэтому возле места проведения работ не должно быть источников открытого огня, даже таких незначительных, как зажигалки и зажженные сигареты.
- Запрещено использование карбида в гранулах до 2 мм или карбидной пыли, так как она растворяется очень быстро, что приводит к выделению большого количества газа. Из-за этого в генераторе образуется сверхвысокое давление и может произойти взрыв.
- Запрещена работа болгаркой или электросварочным аппаратом вблизи газосварочных работ и мест установки карбидных барабанов.
- Вещество должно храниться в сухом и герметичном месте, в котором нет водопроводов, канализационных труб и, тем более, газового оборудования.
- Карбидная пыль при попадании вызывает раздражение кожи, глаз, слизистых оболочек. Работа с этим веществом должна проходить с применением средств индивидуальной защиты – очков, перчаток и респиратора.
- При попадании карбида на кожу или в глаза его необходимо промыть большим количеством теплой воды, а затем аккуратно удалить остатки карбида пинцетом или влажным тампоном.
- При работе с карбидом в мастерской все сварочное оборудование должно быть размещено в отдельных частях помещения, система вентиляции помещения должна обеспечивать отвод горючих газов, а помещение должно быть освобождено от горючих материалов.
- Ацетиленовые генераторы запрещено устанавливать в подвальных помещениях и жилых зданиях.
- Перед запуском генератор следует осмотреть на предмет отсутствия видимых трещин и вмятин корпуса.
- Во время проведения работ генератор должен оставаться в вертикальном положении, манометр должен быть исправен и хорошо виден сварщику или его помощнику.
- По окончании работы оставшийся в генераторе раствор карбида должен быть выработан целиком, а образовавшаяся известь утилизирована.
- Повторное использование мокрых кусков карбида не допускается;
- Запрещено вскрывать генератор под давлением (во время продолжающейся реакции).
- Баллоны для ацетилена хранятся и перевозятся со специальными предохранительными колпаками на клапанах.
Соблюдение этих простых правил позволит обеспечить собственную безопасность и безопасность людей, находящихся вблизи объекта работ.
Карбид следует покупать в проверенных магазинах сварочного оборудования, поскольку приобретение некачественного карбида может затруднить проведение сварочных работ. Можно также заказать его в интернет-магазинах. Цена карбида варьируется от 75 до 190 рублей за килограмм, в зависимости от производителя.
Если имеется необходимость в регулярном использовании оборудования для газовой сварки и резки, лучше купить профессиональное оборудование, изготовленное на промышленном предприятии. Применение самодельных генераторов чревато получением тяжелых травм и угрозой для жизни.
Стоимость
На рынке карбид кальция можно приобрести по цене 80 рублей за килограмм. Продают данную смесь в бочках или специальных мешках. Ненамного дороже вещество с кремнием. Его стоимость составляет 82 рубля за килограмм. А вот, карбид вольфрама обойдется в 1400 рублей за кило. Причем, может быть установлен минимальный вес покупки, например, от 10 кг. Карбид бора будет стоить еще дороже — от 2000 рублей, причем фасовка начинается от 35 килограмм. Стоимость же соединений с гафнием или молибденом оговаривается с поставщиком отдельно.
| Карбид кальция | |
| Общие | |
| Систематическое наименование | Кальция карбид |
| Хим. формула | CaC2 |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса | 64,0994 (±0,004) г/моль |
| Плотность | 2,22 г/см³ |
| Термические свойства | |
| Т. плав. | 2160 °C |
| Т. кип. | 2300 °C |
| Структура | |
| Координационная геометрия | 6 |
| Кристаллическая структура | Тетрагональная |
| Классификация | |
| Рег. номер CAS | 75-20-7 |
| PubChem | 6352 |
| Рег. номер EINECS | 200-848-3 |
| SMILES | |
| RTECS | EV9400000 |
| ChemSpider | 6112 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Карби́д ка́льция
(углеро́дистый ка́льций, ацетилени́д кальция) — CaC2 — в чистом виде белое кристаллическое вещество. Соединение кальция с углеродом.
Применение вещества
Кальция карбид активно применяется в промышленности. Он является катализатором в сфере синтеза органических соединений. С его помощью стало возможным синтезировать каучук за более низкую цену. Однако для этого вначале необходимо провести необходимые химические реакции для синтеза собственного карбида, а уже потом — каучука. Все больше химиков задаются вопросом о том, где найти карбид в природе, чтобы облегчить себе работу.
Карбид нашел свое применение в садоводстве. На его основе фермеры получают удобрение под названием цианид кальция. Применяется для улучшения роста корневой системы саженцев и взрослых растений.
Получение [ править | править код ]
В настоящее время получают прокаливанием в электрических печах (температура 1900—1950 °C) смеси оксида кальция с коксом.
C a O + 3 C → C a C 2 + C O >> 2>
Полученный таким образом технический продукт имеет грязно-серый цвет вследствие загрязнения углём и другими красящими примесями. Он содержит также примеси фосфида и сульфида кальция, вследствие чего такой карбид кальция и полученный из него ацетилен имеют неприятный запах.
Читать также: Сравнить стиральные машинки по характеристикам
Физические свойства [ править | править код ]
- Бесцветные тетрагональные кристаллы.
- Плотность: 2,2 (+20 °C, г/см 3 ).
- Удельная теплоёмкость при постоянном давлении (в Дж/г·K): 0,92 (+20—325 °C).
- Стандартная энтальпия образования ΔfH (298 К, кДж/моль): −62,8 (т).
- Стандартная энергия Гиббса образования ΔfG (298 К, кДж/моль): −67,8 (т).
- Стандартная энтропия образования S (298 К, Дж/моль·K): 70,3 (т).
- Стандартная мольная теплоёмкость Cp (298 К, Дж/моль·K): 62,34 (т).
- Энтальпия плавления ΔHпл (кДж/моль): 32,2 [1] .
Внешний вид и характеристики технического карбида кальция [ править | править код ]
Карбид кальция получают сплавлением в электрических печах кокса и негашеной извести. Расплавленный карбид кальция выпускается из печи в специальные формы — изложницы, в которых он затвердевает. Застывший карбид кальция дробится и сортируется на куски определённых размеров.
Технический карбид кальция представляет собой твёрдое кристаллическое вещество. По внешнему виду карбид кальция представляет собой твёрдое вещество тёмно-серого или коричневого цвета. Он даёт кристаллический излом серого цвета с различными оттенками в зависимости от чистоты. Карбид кальция жадно поглощает воду. При взаимодействии с водой даже на холоде карбид кальция разлагается с бурным выделением ацетилена и большого количества тепла. Разложение карбида кальция происходит и под влиянием атмосферной влаги.
По ГОСТ 1460-56 установлены следующие размеры (грануляция) кусков карбида кальция: 2×8; 8×15; 15×25; 25×80. Технический карбид кальция содержит до 80 % химически чистого карбида кальция, остальное составляют примеси — негашеная известь, углерод, кремнекислота и другое [3] .