Общие сведения
Цикл охлаждения, шаг 1. Горячий хладагент, сжатый компрессором, охлаждается окружающим воздухом и конденсируется в теплообменнике оконного кондиционера
Удельный объем — это объем на единицу массы. Это свойство веществ часто используется в термодинамике. Удельный объем — величина, обратная плотности. Его находят, разделив объем на массу. Удельный объем газов можно найти также по их плотности, температуре и молекулярной массе. Величину объема на единицу массы используют чаще, но иногда, говоря об удельном объеме, подразумевают отношение объема к молекулярной массе. Обычно из контекста понятно, о каком удельном объеме идет речь. Единицы удельного объема по массе отличаются от единиц удельного объема по молекулярной массе, поэтому можно понять, о каком удельном объеме идет речь, глядя на единицы, в которых эта величина измеряется. Удельный объем по массе измеряют в м³/кг, л/кг, или фут³/фунт, в то время как удельный объем по молекулярной массе измеряют в м³/моль и производных единицах. В некоторых случаях удельный объем по молекулярной массе называют молярным объемом
или
удельным молярным объемом
.
Объем, масса, плотность, удельный объем. Приведение к нормальным и стандартным условиям и пересчет
Приведение к нормальным и стандартным условиям
Единицей измерения объема газа является кубический метр (м³). Измеренный объем приводится к нормальным физическим условиям.
Нормальные физические условия: давление 101 325 Па, температура 273,16 К (0 °С).
Стандартные условия: давление 101 325 Па, температура 293,16 К (+20 °С).
В настоящее время эти обозначения выходят из употребления. Поэтому в дальнейшем следует указывать те условия, к которым относятся объемы и другие параметры газа. Если эти условия не указываются, то это значит, что параметры газа даны при 0 °С (273,16 °К) и 760 мм рт. ст. (1,033 кгс/см²). Иногда объем газа (особенно в иностранной литературе и нормах) при пользовании системой СИ приводится к 288,16 °К (+15 °С) и давлению 1 бар (105 Па).
Если известен объем газа при одних условиях, то пересчитать его в объемы при других условиях можно с помощью коэффициентов, приведенных следующей таблице.
Коэффициенты для пересчета объемов газа из одних условий в другие
| Температура и даление газа | 0 °С и 760 мм рт. ст. | 15 °С и 760 мм рт. ст. | 20 °С и 760 мм рт. ст. | 15 °С (288,16 °К) и 1 бар |
| 0 °С и 760 мм рт. ст. (норм. условия) | 1 | 1,055 | 1,073 | 1,069 |
| 15 °С и 760 мм рт. ст. (в зар. литературе) | 0,948 | 1 | 1,019 | 1,013 |
| 20 °С и 760 мм рт. ст. (ст. условия) | 0,932 | 0,983 | 1 | 0,966 |
| 15 °С (288,16 °К) и 1 бар (СИ) | 0,936 | 0,987 | 1,003 | 1 |
Для приведения объемов газа к 0 °С (273,16 °К) и 760 мм рт. ст. (1,033 кгс/см²), а также к 20 °С (293,16 °К) и 760 мм рт. ст. (1,033 кгс/см²) могут быть применены следующие формулы:
где V0 °С и 760 мм рт. ст. — объем газа при 0 °С и 760 мм рт. ст., м³; V20° С и 760 мм рт. ст. — объем газа при 20 °С и 760 мм рт. ст., м³; VP — объем газа в рабочих условиях, м³; р — абсолютное давление газа в рабочих условиях, мм рт. ст.; Т — абсолютная температура газа в рабочих условиях, °К.
Пересчет объемов газа, приведенных к 0 °С и 760 мм рт. ст., а также к 20 °С и 760 мм рт. ст., в объемы при других (рабочих) условиях можно производить по формулам:
Любой газ способен расширяться. Следовательно, знание объема, который занимает газ, недостаточно для определения его массы, так как в любом объеме, целиком заполненном газом, его масса может быть различной.
Масса — это мера вещества какого-либо тела (жидкости, газа) в состоянии покоя; скалярная величина, характеризующая инерционные и гравитационные свойства тела. Единицы массы в СИ — килограмм (кг).
Плотность, или масса единицы объема, обозначаемая буквой p, — это отношение массы тела m, кг, к его объему, V, м³:
p = m/V
или с учетом химической формулы газа:
p = M/VМ = M/22,4,
где M — молекулярная масса, VМ — молярный объем.
Единица плотности в СИ — килограмм на кубический метр (кг/м³).
Зная состав газовой смеси и плотность ее компонентов, определяем по правилу смешения среднюю плотность смеси:
pсм = (p1V1 + p2V2 + … + pnVn)/100,
где p1, p2, …, pn — плотность компонентов газового топлива, кг/м³; V1, V2, …, Vn — содержание компонента, об. %.
Величину, обратную плотности, называют удельным, или массовым, объемом (ν) и измеряют в кубических метрах на килограмм (м³/кг).
Как правило, на практике, чтобы показать, на сколько 1 м³ газа легче или тяжелее 1 м³ воздуха, используют понятие относительная плотность d, которая представляет собой отношение плотности газа к плотности воздуха:
d = p/1,293
и
d = M/(22,4×1,293).
Использование удельного объема
Если сравнить твердые вещества, жидкости и газы, то легко заметить, что изменить плотность или удельный объем газов проще всего. Кстати, когда говорят о твердых веществах и жидкостях, чаще всего используют плотность, а говоря о газах чаще используют удельный объем. Удельный объем также обычно используют при работе с системами, в которых вещество или вещества присутствуют в нескольких разных агрегатных состояниях.
Цикл охлаждения, шаг 2. Охлажденный хладагент в форме жидкости проходит через капиллярную трубку и попадает в испаритель (теплообменник, показанный на иллюстрации). Теплый воздух из комнаты проходит через холодный испаритель, где охлаждается
Двухфазные системы
Двухфазные системы — это системы, которые состоят из вещества, находящегося в двух разных агрегатных состояниях, например жидкость–газ, или жидкость–твердое тело. Смесь льда и воды в чашке — хороший пример системы жидкость–твердое тело. Системы жидкость–газ можно найти в котельной электростанции, которая работает на газе, в атомном реакторе или в кондиционере. В некоторых случаях интересно наблюдать за двухфазной системой, например чтобы узнать, как она изменяется при изменении температуры или давления. Нередко интерес представляют изменения в объеме вещества при изменении агрегатного состояния этого вещества. В этом случае используют удельный объем. В общем, удельный объем удобно использовать, чтобы описать свойства двухфазной системы.
Вначале рассмотрим примеры двухфазных систем и их применения в повседневной жизни и в технике. Затем обсудим применение удельного объема.
Системы отопления, вентиляции и кондиционирования воздуха
Цикл охлаждения, шаг 3. Хладагент в газообразном состоянии выходит из испарителя и попадает в компрессор, где его сжимают. При этом давление в хладагенте увеличивается. После он попадает в конденсатор (теплообменник), и цикл охлаждения повторяется
В большинстве установок отопления, вентиляции и кондиционирования (ОВК или по-английски HVAC) используются на двухфазные системы. При отоплении воду иногда нагревают до тех пор, пока она не превращается в пар, который подается по трубам системы отопления для нагрева помещения, конденсируется в радиаторах отопления в возвращается в котел в виде жидкости. Во многих системах отопления по трубам циркулирует горячая вода. В таких системы отопления для нагрева воды используют бойлеры. Воду в бойлере нагревают, сжигая топливо. Часто это ископаемое топливо, например уголь или природный газ.
С другой стороны, в процессе охлаждения используют вещество, называемое холодильным агентом или хладагентом. В процессе работы это вещество находится попеременно в двух фазах — жидкой и газообразной. Вначале газообразный хладагент охлаждают в теплообменнике, называемом конденсатором, до тех пор, пока он не переходит в жидкое состояние. Конденсатор находится вне охлаждаемого помещения. При этом хладагент конденсируется на стенках теплообменника, отдавая тепло в окружающую среду. После этого хладагент сжимают компрессором и пропускают по трубам через находящийся в охлаждаемом помещении другой теплообменник, называемый испарителем. В нем жидкий хладагент превращается в газ. На это преобразование требуется очень много тепла, которое и отбирается в охлаждаемом помещении. В газообразном состоянии хладагент возвращается в первый теплообменник, и весь процесс повторяется.
Уличный блок сплит-системы кондиционирования воздуха
Переход жидкости в газообразное состояние требует большое количество энергии. В процессе охлаждения система забирает тепло из комнаты для нагрева хладагента, и благодаря этому охлаждает помещение. Конденсатор в кондиционере охлаждает газ (хладагент), отдавая тепло в окружающую среду, то есть на улицу.
Домашние холодильники и промышленные холодильные камеры работают по такому же принципу. Некоторые устройства отопления, вентиляции и кондиционирования объединены в одну систему. В других случаях обогреватель и кондиционер представляют собой отдельные устройства.
Солнечные коллекторы используют для охлаждения
Солнечные коллекторы
Солнечные коллекторы работают по похожему принципу. Панели солнечных коллекторов собирают солнечную энергию, которая используется для нагрева воздуха или жидкости, например воды или антифриза. Полученную тепловую энергию используют для обогрева помещений или для нагрева воды.
Тепловые трубки — это высокоэффективные теплопередающее устройства. Их высокая теплопередача обеспечивается благодаря большому количеству энергии, которая расходуется на парообразование и выделяется при конденсации жидкости внутри них
Тепловые трубки
Процесс работы тепловых трубок похож на работу кондиционера, с разницей в том, что вместо охлаждения воздуха охлаждают твердые поверхности, например металлические. Тепло этих поверхностей нагревает жидкость в трубках до тех пор, пока эта жидкость не испаряется. В остальном процесс идентичен: газ охлаждается и конденсируется, и его снова возвращают в трубки для нагревания. Примеры охлаждающих веществ — это гелий, спирт, и ртуть. Нередко такие системы используют внутри электронных приборов, например компьютеров, для охлаждения электронных элементов, подверженных сильному нагреванию. Также эти системы используют в космосе в экстремальных температурных условиях.
Устройство и работа двухфазных систем
При определенных условиях вещество в двухфазных системах обычно может находиться в этой системе одновременно в двух разных фазах. Если же эти условия не соблюдены, то вещество в системе может быть только в одном агрегатном состоянии, как мы подробно опишем ниже.
В двухфазных системах изменения температуры вызваны изменением давления, а не удельного объема. Иногда, наоборот, давление и температура постоянные, а удельный объем изменяется. Это происходит, когда при постоянном давлении в системе поддерживается температура, которая позволяет веществу существовать одновременно в двух фазах. При таких условиях, как только система достигает нужной температуры, если эта температура не изменяется, то жидкость постепенно переходит в газообразное состояние, и удельный объем в результате увеличивается. Конечно, при этом изменяется и общий объем вещества в системе. Сама система также должна быть рассчитана на такое увеличение объема. С другой стороны, в системах с ограниченным объемом и массой, где невозможно изменять удельный объем, ситуация выглядит иначе. Ниже мы рассмотрим принцип работы такой системы на примере скороварки. Но вернемся к нашей системе, которая допускает изменения в удельном объеме. Удельный объем в ней будет увеличиваться до тех пор, пока вся жидкость не испарится и система вновь не достигнет равновесия.
Чтобы спроектировать котлы и турбины, используемые в электростанциях, например работающих на природном газе, как на фотографии, необходимо понимание теплового обмена и изменения давления в двухфазных системах
Только что мы познакомились с системами с неизменным давлением. Теперь рассмотрим систему с неизменной температурой и изменяющимся давлением. Для каждого вещества существует диапазон давлений, при которых оно может находиться только в газообразном состоянии. Также существует диапазон давлений, при котором вещество может быть одновременно и жидкостью и газом. Стоит заметить, что при изменении давления изменяется также и удельный объем.
Порог, после которого вещество не может быть одновременно в двух агрегатных состояниях, существует также и для жидкости. Порог температуры называют критической температурой, а порог давления — критическим давлением. Сочетание температуры и давления, при которых исчезают различия в свойствах жидкой и газообразной фаз вещества, в термодинамике называют критической точкой.
Физические свойства жидкости
К основным физическим свойствам жидкости, которые рассматриваются в гидродинамике, относятся плотность, удельный вес, удельный объем, температурное расширение, сжимаемость и вязкость.
Плотность — это отношение массы вещества к его объему:
На плотность жидкости влияют температура и давление. Значения плотности некоторых жидкостей приведены ниже:
Удельный вес — это отношение веса жидкости к занимаемому объему:
Удельный объем жидкости — объем единицы массы этой жидкости:
Температурное расширение — свойство жидкости изменять свой объем при изменении температуры. С ростом температуры объем жидкости увеличивается и наоборот. Различные жидкости при увеличении температуры на одну и ту же величину увеличиваются в объеме по разному. Поэтому свойство жидкости увеличиваться в объеме с увеличением температуры характеризуется коэффициентом температурного расширения Bт, который показывает изменение единицы объема данной жидкости при изменении ее температуры на 1 К.
Увеличение объема при нагревании рассчитывается по уравнению:
дельта V= Bт*V0*дельта Т
где V0 начальный объем жидкости; дельта Т— изменение температуры.
В расчетах ДВС коэффициент температурного расширения считают постоянным, хотя на самом деле он зависит от условий нагревания или охлаждения, давления и начальной температуры.
Сжимаемость — свойство жидкости изменять объем при изменении давления.
дельта V = Bр*V0*дельта р,
где дельта V— изменение объема; дельта р — изменение давления; Вр — коэффициент объемного сжатия.
Коэффициент объемного сжатия показывает изменение единицы объема жидкости при изменении давления на 1 Па. Он зависит от условий сжатия, температуры и начального давления. При расчетах эта зависимость не учитывается.
Коэффициент объемного сжатия для воды равен 5 * 10^-4 1/Па, для нефтепродуктов — 7*10^-4 1/Па, для ртути — 0,3*10^-4 1/Па.
Ввиду незначительных величин жидкости считаются несжимаемыми.
Вязкость — свойство жидкости оказывать сопротивление перемещению одной ее части относительно другой.
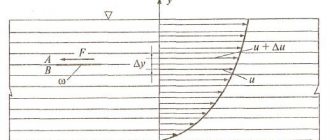
Рис. Схема изменения скорости жидкости, заключенной между неподвижной (1) и подвижной (2) пластинами
Если плоскость 2, находящаяся на расстоянии б от плоскости 1, под действием силы F перемещается со скоростью V0, то слои жидкости, находящиеся между плоскостями, перемещаются с разными скоростями. При этом максимальная скорость V0 в точках контакта с плоскостью 2, минимальная (вплоть до нуля) в точках контакта с плоскостью 1.
Температура, давление и удельный объем
В термодинамике давление, температура и удельный объем — три величины, связанные между собой и зависящие друг от друга. Так как эти величины легко найти, их удобно использовать для описания термодинамических систем. Как мы описали выше, если вещество находится в одной фазе, то изменение давления или изменение температуры вызывают увеличение или уменьшение удельного объема. Как этот удельный объем изменяется, зависит от вещества, но для большинства газов увеличение давления при постоянной температуре вызывает уменьшение удельного объема. С другой стороны, увеличение температуры при постоянном давлении чаще всего увеличивает удельный объем. Такая зависимость также позволяет контролировать давление или температуру при помощи изменения удельного объема. Именно по такому принципу и работает скороварка.
Температура кипения воды в скороварке увеличивается до 121 °C (250 °F) на уровне моря при давлении, которое выше атмосферного давления на уровне моря на 1 бар или примерно 15 фунтов на квадратный дюйм
Плотности и удельные объёмы некоторых веществ[ | ]
В таблице приведены плотности и удельные объёмы для некоторых веществ. Значения указаны для стандартных температуре и давлении: 0°С (273,15 К) и 1 атм (101,325 кПа или 760 мм рт. ст.).
| Название вещества | Плотность, (кг/м3) | Удельный объём, (м3/кг) | Название вещества | Плотность, (кг/м3) | Удельный объём, (м3/кг) |
| Воздух | 1.225 | 0,816 | Двуокись углерода | 1,977 | 0,506 |
| Водяной лёд | 916,7 | 0,00109 | Хлор | 2,994 | 0,334 |
| Жидкая вода | 1000 | 0,00100 | Водород | 0,0899 | 11,12 |
| Морская вода | 1030 | 0,00097 | Метан | 0,717 | 1,39 |
| Ртуть | 13546 | 0,00007 | Азот | 1,25 | 0,799 |
| Фреон R-22* | 3,66 | 0,273 | Водяной пар* | 0,804 | 1,24 |
| Аммиак | 0,769 | 1,30 | |||
| * — значения указаны для нестандартных температуры и давления | |||||