Остаточное давление в баллонах — статья ГазЗаЧас
Главная » Статьи » Остаточное давление в баллонах
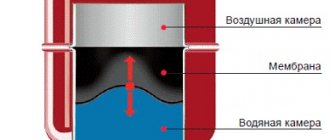
При эксплуатации баллонов полностью выбирать (расходовать) технический газ, который содержится в них, запрещено по технике безопасности. В емкости должно оставаться остаточное давление. Но насколько это необходимо, и что дает это остаточное давление?
Остаточное давление в баллоне должно составлять не менее пол-атмосферы (0,05 МПа). Данного количества достаточно, чтобы при необходимости проверить струю на газоанализаторе и выяснить, какой газ содержался в баллоне. Это позволит избежать смешивания горючих газов с кислородом, ведь даже незначительные остатки метана, пропана, ацетилена, масла могут спровоцировать взрыв. Согласитесь, чтобы избежать такой невеселой перспективы, не грех и перестраховаться.
Конечно, подобные риски сведены к минимуму, ведь любой мало-мальски знающий человек, скажет, что спутать баллоны для горючих и негорючих газов практически невозможно. Это все равно, что не отличить бегемота от слона. Однако находчивость человека не знает границ, и случаи, когда баллоны использовали не под предназначенные газы, известны. Кроме того, остаточное давление – гарантия того, что баллон не наполнился посторонними жидкостями и веществами (например, воздухом, маслом, водой) в то время, когда он не использовался по прямому назначению. Многие не знают, но при взаимодействии обычного моторного масла с кислородом может произойти взрыв. Кислородные баллоны без остаточного давления к заправке не прнимаются, т.к. даже капля масла, попавшая внуть баллона, может спровоцировать взрыв!
Можно ли «реанимировать» газовый баллон без остаточного давления и сделать его пригодным для эксплуатации? Это возможно, однако в этом случае требуется тщательный внутренний осмотр баллона. Если вы не хотите откручивать вентиль и заглядывать в недра своих газовых баллонов с помощью электрических ламп, чтобы удостовериться, что туда не попало масло, не забывайте про необходимость остаточного давления.
Все статьи
На нашем сайте Вы можете сделать заказ необходимого Вам оборудования в городах и регионах: Москва, Санкт-Петербург, Новосибирск, Екатеринбург, Нижний Новгород, Казань, Челябинск, Ростов-на-Дону, Уфа, Красноярск, Краснодар.
8(800)500-49-17 — Звонок по России бесплатный
gazzachas.ru
Способы получения кислорода
В основном кислород получают тремя способами:
- разделение воздуха путем низкотемпературной ректификации (глубокого охлаждения);
- разложение воды путем электролиза (пропускание электрического тока);
- химический способ.
Из атмосферного воздуха его получают методом глубокого охлаждения, как побочный продукт при получении азота.
Также O2 добывают путем пропускания электрического тока через воду (электролиз воды) с попутным получением водорода.
Химические способ получения малопроизводителен, а, следовательно, и неэкономичен, он не нашел широкого применения и используются в лабораторной практике.
Наверно многие помнят химический опыт, когда в колбе нагревают марганцовку (перманганат калия KMnO4), а потом выделяющийся в процессе нагрева газ собирают в другую колбу?
2KMnO4 = K2MnO4 + MnO2 + O2 ↑
А весь фокус был, когда в данную колбу помещали тлеющую лучинку и она вспыхивала ярким пламенем и учитель объяснял, что выделившийся газ — O2, который поддерживает горение. И что процесс горения — это не что иное, как процесс окисления.
Характеристики
Емкости изготавливаются из стальной трубы с пределами прочности не ниже 65 кг/кв. мм, а внутренняя поверхность не имеет дефектов и абсолютно гладкая. Толщина стенок не менее 6 мм и не более 9 мм, с одной стороны изделие имеет закругленную форму, а с другой — запаян вентиль, к которому присоединяется редуктор.
Заправка баллонов кислородом осуществляется только в вертикальном положении, для чего в нижней части устанавливается башмак. После заправки на вентиль одевается предохранительный колпак, чтобы защитить горловину от механических повреждений при транспортировке.
Максимальное давление
Разной емкости баллоны выдерживают определенную нагрузку при закачивании в них кислорода:
- 40 л — 150 кг/см²;
- 50 л — 200 кг/см².
Толщина стенок зависит от производителя, но рекомендуется не ниже стандарта 6—8 мм.
Вес
Сколько же весит заправленный кислородный баллон, вычислить это не так уж и трудно, зная массу всех составляющих:
- башмак — не более 5,2 кг;
- резиновое кольцо — 300 г;
- защитный колпак из металла — 1,8 кг;
- масса закаченного газа в зависимости от давления — 8—12 кг.
После непродолжительных подсчетов имеем такой результат: 40 л заполненный баллон весит 67 кг, а на 50 л — не более 100 кг, что зависит от колпака, который выпускают и из прочного пластика.
Объем
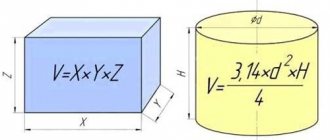
Для того чтобы узнать сколько закачено кислорода в баллоне в м3, существуют специальные формулы, поэтому в емкости, рассчитанной на 40 л, вмещается при давлении в 150 кг/см² — 150х40=6 тыс. литров или 6 куб. метров. Для баллона на 50 л и с давлением в 200 кг/ см2 получаем 10 м3.
Комплектация
Основным дополнительным элементом емкости для кислорода является вентиль. Изготавливают его из латуни. Поверх вентиля обязательно устанавливается защитный колпак, он может быть алюминиевым или пластмассовым. Обычно колпак идет, как неотъемлемая часть. Но теряются они часто, так что защитное приспособление может быть изготовлено из любого материала своими руками. Здесь важна надежность и герметичность. В сам баллон вентиль вкручивается посредству конической резьбы
Второй по значимости элемент – это башмак. Именно на него ложится вся весовая нагрузка. Изготавливается он из стальной ленты, которую формируют по сечению в квадрат. ГОСТом точно не определенно, как он должен закрепляться на баллоне, поэтому некоторые производители приваривают его, другие впрессовывают.
История открытия кислорода
Открытие кислорода приписывают Джозефу Пристли (Joseph Priestley). У него была лаборатория, оборудованная приборами для собирания газов. Он испытывал его физиологическое действие на себе и на мышах. Пристли установил, что после вдыхания газа некоторое время ощущается приятная легкость. Мыши в герметически закрытой банке с воздухом задыхаются быстрей, чем в банке с O2. Поскольку Пристли был приверженцем флогистонной теории он так и не узнал, что оказалось у него в руках. Он только описал этот газ, даже не догадываясь, что он описал. А вот лавры открытия кислорода принадлежат Антуан Лоран Лавуазье (Antoine Laurent de Lavoisier), который и дал ему имя.
Лавуазье, поставил свой знаменитый опыт, продолжавшийся 12 дней. Он нагревал ртуть в реторте. При кипении образовывалась ее красная окись. Когда реторту охладили, оказалось, что воздуха в ней убыло почти на 1/6 его объема, а остаток ртути весил меньше, чем перед нагревом. Но когда разложили окись ртути сильным прокаливанием, все вернулось: и недостача ртути, и «исчезнувший» кислород.
Впоследствии Лавуазье установил, что этот газ входит в состав азотной, серной, фосфорной кислот. Он ошибочно полагал, что O2 обязательно входит в состав кислот, и поэтому назвал его «оксигениум», что значит «рождающий кислоты». Теперь хорошо известны кислоты, лишенные «оксигениума» (например: соляная, сероводородная, синильная и др.).
Сфера использования
Сжатый кислород – популярный газ, область применения которого зависит от вида сырья. Медицинское вещество используют во время реанимации пациентов. Элемент оказывает благоприятное воздействие на сердце и легкие, поэтому часто назначают лечебные процедуры при проблемах со здоровьем. Компонент берут для насыщения коктейлей при кислородном голодании.
Сферы использования Источник krsk.au.ru
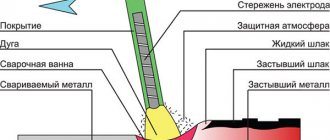
Технический газ быстро нагревается и долго поддерживает высокие температуры. Полученная сплошная струя прожигает металл любой плотности, что позволяет разрезать или спаивать детали. Характеристика полезна как в строительстве, так и в бытовом использовании. В металлургии вещество усиливает КПД печей, чем улучшает качество готовой продукции.
В химической промышленности применяют во время производства сложных кислот и взрывчатки. В целлюлозной отрасли кислородом очищают и отбеливают бумагу, в рыбной – обогащают пруды. В авиации газ участвует в окислении двигательного топлива.
Применение в строительстве Источник ugra.ru